
��һ�������£���һ���Ϊ2L�ĺ����ܱ������г���2mol A��1mol B���������·�Ӧ��
2A��g��+B  3C��g������H=��QkJ/mol��Q>0��������60s�ﵽƽ�⣬���B���ʵ���
3C��g������H=��QkJ/mol��Q>0��������60s�ﵽƽ�⣬���B���ʵ���
Ϊ0.2mol�����жԸ�ƽ���������ȷ���� �� ��
A����C��Ũ�ȱ仯��ʾ�÷�Ӧ����Ϊ2��4mol��L-1��min-1
B����ʹ������Ϊ1L����C�����ʵ���һ������
C���ﵽƽ�⣬��÷ų�����ΪxkJ����x=Q
D�����������ٳ���1mol C�����´ﵽƽ�⣬A������������ֲ��䣬��BΪ��̬
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и��黯�����У����������Ժ��ֱ�����ϣ�ֻҪ������һ��������ȫȼ��ʱ����
O2������������ˮ�������������( )
A��CH4��C2H6 B��C2H2��C6H6 C��C2H4��C4H6 D��C2H4��C3H4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���м�����������ԭ��Ӧ�����������ȷ�Ӧ����
A����Ƭ��ϡ���ᷴӦ
B����������ʯ��ʯ
C�����ȵ�̼�������̼�ķ�Ӧ
D�������������е�ȼ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1��������100mL 0.1mol��L-1 H2C2O4�����ᣬҲ���Ҷ��ᣩ��ҺpH=2��
�ٽ���ϡ��10������ҺpH 3���<������>����=��������ʱͬ���0.01 mol��L-1ϡ��������ֱ������п��Ӧ��ϡ����ų���������� ����ࡱ�����١�����ȡ�����
�������м����������ƹ��壬��������������� ��
A.c(H2C2O4) B.c(OH-) C.ˮ�����ӻ� D.��Һ������
��2����������������Һ����0.01mol/L��CH3COOH��Һ����pH=2��ϡ���ᡢ
��pH=12��ʯ��ˮ����0.01mol/L��KOH��Һ��
����ˮ�ĵ���̶������� �����ţ�������pH=2�Ĵ�����Һ�����Һ�������ϣ�������ҺpH 7���<������>����=������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��֪W��X��Y��ZΪ������Ԫ�أ�W��Z�����壬X��Y��Zͬ���ڣ�W����̬�⻯����ȶ�
�Դ���Z����̬�⻯����ȶ��ԣ�X��YΪ����Ԫ�أ�X�������ӵ�������С��Y�������ӵ������ԡ�����˵����ȷ���ǣ� ��
A��W����̬�⻯��ķе�һ������Z����̬�⻯��ķе�
B��W��X�γɵĻ�������ֻ�����Ӽ�
C��X��Y��Z��W��ԭ�Ӱ뾶���μ�С
D����W��Yԭ���������5��������γɻ�����Ļ�ѧʽһ��ΪY2W3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��1 mol A(g)��2 mol B(g)����2Lij�ܱ������У���һ���¶��·�����Ӧ��
A(g)+B(g)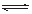 C(g)+D(g)�����ﵽƽ�⡣C�����������ʱ��仯����ͼI������b��ʾ����Ӧ�����е������仯��ͼII��ʾ������˵������ȷ���ǣ� ��
C(g)+D(g)�����ﵽƽ�⡣C�����������ʱ��仯����ͼI������b��ʾ����Ӧ�����е������仯��ͼII��ʾ������˵������ȷ���ǣ� ��

A����������Ӧ��ϵ�м����������ѧ��Ӧ��������E1��E2����С
B�����¶��£���Ӧ��ƽ�ⳣ����ֵԼΪ7.36
C�����������£���С��Ӧ�����������ʹ��Ӧ �Ĺ��̰�ͼI��a���߽���
D����Ӧ�ڵ�4���Ӵﵽ��ѧƽ��״̬��0��4���ڣ���A��ʾ�Ļ�ѧ��Ӧ������0.225mol��L-1��s-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������ʵ��������������ԭ�����͵��ǣ� ��
A��������ˮ��Һ�м����������S2��������
B���ȵĴ�����Һȥ������ǿ
C����ѹ�����ںϳɰ���Ӧ
D��500�����ұ����¸����ںϳɰ���Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���ܱ����з������з�ӦaA(g) cC(g)��dD(g)����Ӧ�ﵽƽ����������ѹ����ԭ����һ�룬���ٴδﵽƽ��ʱ��D��Ũ��Ϊԭƽ���1.8��������������ȷ����( )
cC(g)��dD(g)����Ӧ�ﵽƽ����������ѹ����ԭ����һ�룬���ٴδﵽƽ��ʱ��D��Ũ��Ϊԭƽ���1.8��������������ȷ����( )
A��A��ת���ʱ�� B��ƽ��������Ӧ�����ƶ�
C��D������������ D��a �� c��d
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���и�����������������Һ�еķ�Ӧ������ͬһ���ӷ���ʽ��ʾ����
A��Cu(OH)2 + HCl�� Cu(OH)2 + CH3COOH
B��NaHCO3 + H2SO4�� Na2CO3 + HCl
C��NaHCO3 + NaOH�� NaHSO4 + NaOH
D��BaCl2 + H2SO4�� Ba(OH)2 + Na2SO4
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com