
离子反应是中学化学中重要的反应类型。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有________(填序号)。
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)可用图示的方法表示不同反应类型之间的关系。如分解反应和氧化还原反应可表示为下图。请在下面的方框中画出离子反应、置换反应和氧化还原反应三者之间的关系。
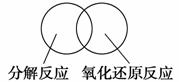
 |
(3)离子方程式是重要的化学用语。下列是有关离子方程式的一些错误观点,请在下列表格中用相应的“离子方程式”否定这些观点。
| ①所有的离子方程式均可以表示一类反应 | |
| ②酸碱中和反应均可表示为H++OH-===H2O | |
| ③离子方程式中凡是难溶性酸、碱、盐均要标“↓”符号 |
(4)试列举出三种不同类别的物质(酸、碱、盐)之间的反应,它们对应的离子方程式都可用“Ba2++SO42-===BaSO4↓”来表示,请写出有关反 应的化学方程式(3个):
应的化学方程式(3个):
①_________________________________________ _____________________;
_____________________;
②______________________________________________________________;
③_____________________________________________________________。
解析 离子反应中一定有离子参与反应或有离子生成,因此一定有电解质(化合物)参与反应或生成。置换反应一定是氧化还原反应,二者有一部分可用离子方程式表示,如Zn+Cu2+===Cu+Zn2+,有的则只能用化学方程式表示,如CuO+H2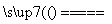 Cu+H2O。
Cu+H2O。
答案 (1)③⑤
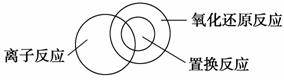
(2)
(3)①2CH3COOH+CaCO3===2CH3COO-+Ca2++H2O+CO2↑
②CH3COOH+OH-===CH3COO-+H2O
③CaCO3+2H+===Ca2++H2O+CO2↑
(4)①BaCl2+H2SO4===BaSO4↓+2HCl
②Ba(OH)2+Na2SO4===BaSO4↓+2NaOH
③NaHSO4+BaCl2===BaSO4↓+HCl+NaCl


科目:高中化学 来源: 题型:
某学习小组探究浓、稀硝酸氧化性的相对强弱的,按下图装置进行试验(夹持仪器已略去)。实验表明浓硝酸能将 氧化成
氧化成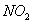 ,而稀硝酸不能氧化
,而稀硝酸不能氧化 。由此得出的结论是浓硝酸的氧化性强于稀硝酸。
。由此得出的结论是浓硝酸的氧化性强于稀硝酸。

可选药品:浓硝酸、3mo/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及二氧化碳
已知:氢氧化钠溶液不与 反应,能与
反应,能与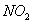 反应
反应
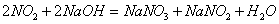
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是
(2)滴加浓硝酸之前先检验装置的气密性,再加入药品,打开弹簧夹后
(3)装置①中发生反应的化学方程式是
(4)装置②的作用是 ,发生反应的化学方程式是
(5)该小组得出的结论依据的试验现象是
(6)试验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别设计了4个试验来判断两种看法是否正确。这些方案中可行的是 (选填序号字母)
a. 加热该绿色溶液,观察颜色变化
b. 向该绿色溶液中通入氮气,观察颜色变化
c. 加水稀释绿色溶液,观察颜色变化
d. 向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化
查看答案和解析>>
科目:高中化学 来源: 题型:
下列解释事实的离子方程式不正确的是 ( )。
A.氨水使酚酞溶液变红:NH4++H2ONH3·H2O+H+
B.醋酸使碳酸钙溶解:CaCO3+2CH3COOH===Ca2++2CH3COO-+CO2↑+H2O
C.草酸溶液使酸性高锰酸钾溶液褪色:2MnO4-+5H2C2O4+6H+===2Mn2++10CO2↑+8H2O
D.向污水中投放明矾,生成能凝聚悬浮物的胶体:Al3++3H2OAl(OH)3(胶体)+3H+
查看答案和解析>>
科目:高中化学 来源: 题型:
醋酸是中学常用的一种弱酸。
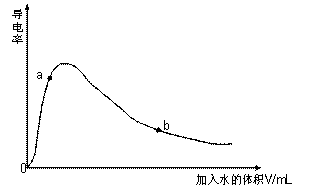
(1)取0.10mol CH3COOH作导电性实验,
测得其导电率随加入的水量变化如图所示:
开始时导电率为0说明: 。
② 比较a、 b点的相关性质(填“>”、“<”、“=”):
n(H+):a b;c(CH3COO-):a b;
完全中和时消耗NaOH的物质的量:a b;
③ 若b点时,溶液中c(CH3COOH)=0.10mol/L,c(H+)=1.3×10-3mol/L,则此时c(CH3COO-)约为 mol/L;计算b点时醋酸的电离平衡常数,写出计算过程 。
(2)已知:H+(aq) + OH-(aq) = H2O(l) △H1=-57.3 kJ/mol
CH3COOH(aq) 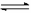 H+(aq) +CH3COO-(aq) △H2=+1.3 kJ/mol
H+(aq) +CH3COO-(aq) △H2=+1.3 kJ/mol
写出稀醋酸与稀烧碱溶液反应的热化学方程式:
。
(3)室温下,取浓度均为0.10mol/L的醋酸与醋酸钠溶液等体积混合后,测得其pH<6,写出混合溶液中的物料守恒关系式 ;并列出其中的离子浓度大小顺序(由大到小) 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子或分子组能大量共存,且满足相应要求的是
( )。
| 选项 | 离子或分子 | 要求 |
| A | K+、NO3-、Cl-、HCO3- | c(K+)<c(Cl-) |
| B | Ca2+、NO3-、SO32-、Cl- | 滴加盐酸立即有气体产生 |
| C | NH4+、Al3+、SO42-、Br- | 逐滴滴加NaOH溶液立即有气体产生 |
| D | Na+、HCO3-、Mg2+、SO42- | 滴加氢氧化钠溶液立即有沉淀产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列反应,可以判断有关物质的氧化性由强到弱的顺序正确的是( )。
①Cl2+2KI===2KCl+I2 ②2FeCl2+Cl2===2FeCl3 ③2FeCl3+2HI===2FeCl2+2HCl+I2 ④H2S+I2===S↓+2HI
A.H2S>I2>Fe3+>Cl2 B.Cl2>Fe3+>I2>S
C.Fe3+>Cl2>H2S>I2 D.Cl2>I2>Fe3+>H2S
查看答案和解析>>
科目:高中化学 来源: 题型:
取一定量的酸性KMnO4溶液依次进行下列实验,有关现象记录如下:
①滴加适量H2O2,紫红色褪去,并有气泡产生;
②再加入适量的PbO2固体,固体溶解,溶液又变为紫红色;
③最 后通入足量的SO2气体。
后通入足量的SO2气体。
请回答下列问题:
(1)KMnO4、H2O2、PbO2氧化性由强到弱的顺序为_________________________ ________________________________ ___________________________;
___________________________;
(2)实验③中的现象为______________________________________________。
(3)实验①、②中反应的离子方程式分别是_____________________________、_________________________________ ______________________________。
______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于化学反应限度的叙述中正确的是( )
A.化学反应的限度都相同 B.可以通过改变反应条件控制化学反应的限度
C.可以通过延长化学反应的时间改变化学反应限度
D.当一个化学反应在一定条件下达到限度时反应即停止
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于铁的叙述正确的是 ( )。
①铁能被磁铁吸引,但纯铁易被腐蚀 ②在人体内的血红蛋白中含有铁元素 ③铁位于元素周期表中第四周期第ⅧB族 ④铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧 ⑤铁与强氧化剂硝酸反应的产物仅是Fe(NO3)3 ⑥不能通过化合反应制得FeCl2和Fe(OH)3
A.①③ B.②④ C.②⑤ D.④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com