
【题目】利用如图所示的实验,探究由两种元素组成的某未知无机矿物甲:

下列叙述错误的是( )
A.硫氰化钾的电子式为![]()
B.甲的化学式为Fe5O7
C.丙中滴加稀硝酸没有气体逸出
D.丙中滴加K3[Fe(CN)6]产生蓝色沉淀
【答案】C
【解析】
A. 硫氰化钾为离子化合物,由K+和SCN-构成,SCN-中C与N之间形成了三对共用电子对,因此硫氰化钾的电子式为![]() ,A项正确;
,A项正确;
B. 由流程可知沉淀丁是CaCO3,n(CaCO3)= ![]() =0.7mol,根据元素守恒可得出甲中的氧原子物质的量,丙溶液中加入硫氰化钾后呈血红色,说明含有Fe3+,且甲中铁的物质的量=
=0.7mol,根据元素守恒可得出甲中的氧原子物质的量,丙溶液中加入硫氰化钾后呈血红色,说明含有Fe3+,且甲中铁的物质的量=![]() =0.5mol,根据铁与氧的物资的量之比可得出甲的化学式;
=0.5mol,根据铁与氧的物资的量之比可得出甲的化学式;
C. 甲的化学式为Fe5O7,可变形为FeO2Fe2O3,与稀硫酸反应后丙溶液中含有亚铁离子,与硝酸发生氧化还原反应;
D. 亚铁离子与铁氰根离子反应生成蓝色沉淀,
A. 硫氰化钾的电子式为![]() ,A项正确,不符合题意;
,A项正确,不符合题意;
B. 沉淀丁是CaCO3,n(CaCO3)= ![]() =0.7mol,根据元素守恒,甲中的氧原子物质的量=n(CO)=n(CO2)= n(CaCO3)= 0.7mol,由丙与硫氰化钾反应呈血红色,可知丙中含有铁离子,则甲中铁的物质的量=
=0.7mol,根据元素守恒,甲中的氧原子物质的量=n(CO)=n(CO2)= n(CaCO3)= 0.7mol,由丙与硫氰化钾反应呈血红色,可知丙中含有铁离子,则甲中铁的物质的量=![]() =0.5mol,甲中铁与氧的物质的量之比为5:7,则甲的化学式为Fe5O7,B项正确,不符合题意;
=0.5mol,甲中铁与氧的物质的量之比为5:7,则甲的化学式为Fe5O7,B项正确,不符合题意;
C. 由B项可知甲的化学式为Fe5O7,可变形为FeO2Fe2O3,与稀硫酸反应后丙溶液中含有亚铁离子,滴加稀硝酸会发生氧化还原反应,还原产物为NO气体,C项错误,符合题意;
D. 丙中亚铁离子与铁氰根离子反应生成铁氰化亚铁蓝色沉淀,D项正确,不符合题意;
答案选C。


科目:高中化学 来源: 题型:
【题目】在密闭容器中发生反应:aX(g)+bY(g)![]() cZ(g)+dW(g)反应达到平衡后,将气体体积压缩到
cZ(g)+dW(g)反应达到平衡后,将气体体积压缩到
原来的一半,当再次达到平衡时,W的浓度为原平衡状态的1.8倍。下列叙述正确的是
A. 平衡向正反应方向移动 B. (a+b)>(c+d)
C. Z的体积分数变大 D. X的转化率变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】容积固定的密闭容器中,达平衡的可逆反应2A(g)![]() 2B(?) + C (?)(△H>0),若随着温度升高,气体平均相对分子质量减小,则下列判断正确的是:( )
2B(?) + C (?)(△H>0),若随着温度升高,气体平均相对分子质量减小,则下列判断正确的是:( )
A. B和C可能都是液体 B. B和C肯定都是气体
C. B和C可能都是固体 D. 若C为固体,则B一定是气体。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型漂白剂(如下图)可用于漂白羊毛等,其中W、Y、Z为不同周期不同主族的短周期元素,W、Y、Z的最外层电子数之和等于X的最外层电子数,W、X对应的简单离子核外电子排布相同。下列叙述正确的是

A.工业上通过电解熔融的WX来制得W
B.W、X对应的简单离子半径顺序为:W>X
C.Y的最高价氧化物对应水化物为弱酸
D.该漂白剂中各元素均满足8电子稳定结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某恒定温度下,在一个2L的密闭容器中,加入4 mol A和2 mol B进行如下反应:3A (g)+2B (g)4C (?)+2D (?),“?”代表状态不确定。反应一段时间后达到平衡,测得生成 1.6 mol C,且反应前后压强之比为5:4,则下列说法正确的是
A.增加C,B的平衡转化率不变
B.此时B的平衡转化率是35%
C.增大该体系的压强,平衡向右移动,化学平衡常数增大
D.该反应的化学平衡常数表达式是K=![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,反应物和生成物均为气体的某反应,反应过程中浓度变化如图(Ⅰ)所示。若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是( )
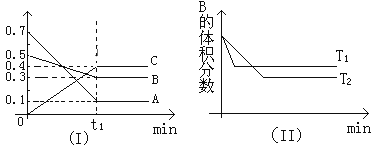
A.在(t1+10)min时,保持其他条件不变,增大压强,平衡向逆反应方向移动
B.在(t1+10)min时,保持压强不变,通入稀有气体,平衡逆反应方向移动
C.T℃时,在相同容器中,若由0.1mol·L-1A、0.3mol·L-1B和0.4mol·L-1C反应,达到平衡后,C的浓度仍为0.4mol·L-1
D.在其他条件不变时,升高温度,正、逆反应速率均增大,且A的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一种利用锂电池“固定CO2”的电化学装置,在催化剂的作用下,该电化学装置放电时可将CO2转化为C和Li2CO3,充电时选用合适催化剂,仅使Li2CO3发生氧化反应释放出CO2和O2。下列说法中正确的是
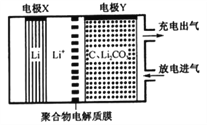
A. 该电池放电时,Li+向电极X方向移动
B. 该电池充电时,电极Y与外接直流电源的负极相连
C. 该电池放电时,每转移4 mol电子,理论上生成1mol C
D. 该电池充电时,阳极反应式为:C+2Li2CO3-4e-=3CO2↑+4Li
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁制品经常进行烤蓝处理,即在铁制品的表面生成一层致密的Fe3O4。某学习小组为了研究烤蓝铁片,分别进行了以下实验操作:
①把一定量烤蓝铁片加工成均匀粉末;
②取m g该粉末,放入28.00 mL 1 mol·L-1的盐酸中,恰好完全反应,生成标准状况下的气体134.4 mL,向溶液中滴入KSCN溶液,无明显现象。
完成下列各题:
(1)将反应后的溶液稀释至100 mL,则溶液中c(Fe2+)=________mol·L-1。
(2)样品中n(Fe)∶n(Fe3O4)=__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对化学平衡移动的分析中,不正确的是
①已达平衡的反应C(s)+H2O(g)![]() CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动 ②已达平衡的反应N2(g)+3H2(g)
CO(g)+H2(g),当增加反应物物质的量时,平衡一定向正反应方向移动 ②已达平衡的反应N2(g)+3H2(g)![]() 2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高 ③有气体参加的反应达到平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动 ④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高 ③有气体参加的反应达到平衡时,若减小反应器容积时,平衡一定向气体体积增大的方向移动 ④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
A.①④B.①②③C.②③④D.①②③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com