
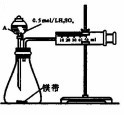
 用如图所示的装置来测定镁与硫酸反应的速率,在锥形瓶中加入0.7g镁带,按图连接好装置,从A中加入20.0mL0.5mol/LH2SO4.记录注射器活塞的位置和相应的时间.实验记录如下:
用如图所示的装置来测定镁与硫酸反应的速率,在锥形瓶中加入0.7g镁带,按图连接好装置,从A中加入20.0mL0.5mol/LH2SO4.记录注射器活塞的位置和相应的时间.实验记录如下:| 时间/s | t | 2t | … |
| 活塞的位置/mL | 25.6 | 36.0 | … |
| 实验序号 | 双氧水体积/mL | 蒸馏水体积/mL | 添加的物质 |
| 1 | 10 | 0 | 4mLFeCl3 |
| 2 | 10 | 2 | 2mLCuCl2 |
分析 (1)镁与硫酸反应生成硫酸镁和氢气;
(2)熟悉化学实验室中常用仪器及作用;
(3)据镁与硫酸反应放热,温度升高,反应速率加快来分析;
(4)①从所给的数据可知:试管1、试管2所用试剂的浓度一样,故研究的是催化剂对反应的催化效果;
②要想研究Fe3+、Cu2+在双氧水分解过程中起催化作用的效果,故可通过测量收集相同体积的氧气所需时间的长短,判断Fe3+、Cu2+在双氧水分解过程中催化效果;
③A中装有10mL双氧水,为减少误差,即减少双氧水的损失,可进行的操作是连接分液漏斗前,直接加到锥形瓶中.
解答 解:(1)镁与硫酸反应生成硫酸镁和氢气,离子反应为Mg+2H+=Mg2++H2↑,
故答案为:Mg+2H+=Mg2++H2↑;
(2)仪器A的用于添加液体药品,故A为分液漏斗,
故答案为:分液漏斗;
(3)0~t时间段与t~2t时间段,化学反应速率快的是t~2t时间段;原因是镁与硫酸反应放热,温度升高,反应速率加快,
故答案为:t~2t;镁与硫酸反应放热,温度升高,反应速率加快;
(4)①从所给的数据可知:试管1、试管2所用试剂的浓度一样,故研究的是催化剂对反应的催化效果,故Fe3+、Cu2+在双氧水分解过程中起催化作用,
故答案为:催化;
②要想研究Fe3+、Cu2+在双氧水分解过程中起催化作用的效果,故可通过测量收集相同体积的氧气所需的时间长短,判断Fe3+、Cu2+在双氧水分解过程中催化效果,
故答案为:收集相同体积的氧气所需时间;
③A中装有10mL双氧水,为减少误差,即减少双氧水的损失,可进行的操作是连接分液漏斗前,直接加到锥形瓶中,
故答案为:连接分液漏斗前,直接加到锥形瓶中.
点评 本题主要考查外界条件对反应速率的影响及催化剂的作用,侧重于学生的实验探究能力的考查,解答时须注意实验的原理,难度中等


科目:高中化学 来源: 题型:解答题
| 化学键 | NO中氮氧键 | Cl-Cl键 | Cl-N键 | N=O键 |
| 键能/KJ/mol | 630 | 243 | a | 607 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
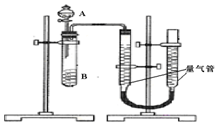 甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.
甲、乙两个实验小组利用KMnO4酸性溶液与H2C2O4溶液反应研究影响反应速率的因素.| 序号 | A溶液 | B溶液 |
| ① | 2mL0.2mol/LH2C2O4溶液 | 4mL0.01mol/LKMnO4溶液 |
| ② | 2mL0.1mol/LH2C2O4溶液 | 4mL0.01mol/LKMnO4溶液 |
| ③ | 2mL0.2mol/LH2C2O4溶液 | 4mL0.01mol/LKMnO4溶液和少量MnSO4 |
| 实验编号 | 1 | 2 | 3 | 4 |
| 水/mL | 10 | 5 | 0 | X |
| 0.5mol/L H2C2O4/mL | 5 | 10 | 10 | 5 |
| 0.2mol/L KMnO4/mL | 5 | 5 | 10 | 10 |
| 时间/s | 40 | 20 | 10 | --- |
| 时间/s | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 温度/℃ | 25 | 26 | 26 | 26 | 26.5 | 27 | 27 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
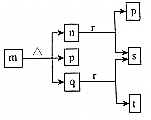 现有三个不同短周期的X、Y、Z、W同种常见元素,其原子序数依次增大,W为金属元素,其余为非金属元素,它们可形成n、q、r三种常见的二元化合物、p、t两种常见三元化合物、m一种常见的四元化合物,它们之间的转化关系如图所示,其中q为无色透明液体,n为无色无味气体,s可使带火星的木条复燃,其余为固体,下列有关说法正确的是( )
现有三个不同短周期的X、Y、Z、W同种常见元素,其原子序数依次增大,W为金属元素,其余为非金属元素,它们可形成n、q、r三种常见的二元化合物、p、t两种常见三元化合物、m一种常见的四元化合物,它们之间的转化关系如图所示,其中q为无色透明液体,n为无色无味气体,s可使带火星的木条复燃,其余为固体,下列有关说法正确的是( )| A. | 离子半径:W+>Z2- | |
| B. | Y的非金属性强于Z,故YX4的热稳定性强于q | |
| C. | n和少量t反应生成m,m还可以和t反应生成p和q | |
| D. | 把少量r投入到FeSO4溶液中,产生无色气体和白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含金属元素的离子可能是阴离子 | |
| B. | 非金属元素组成的化合物可能含有离子键 | |
| C. | 化合物中所含化学键断裂时,一定发生了化学反应 | |
| D. | 用坩埚钳夹住仔细打磨过的铝箔在酒精灯上加热,融化的铝并不滴落 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 己知异丙苯的纺构简式为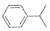 ,则异丙苯中碳原子可能处于同一平面 ,则异丙苯中碳原子可能处于同一平面 | |
| B. | 分子式为C4H9Cl的有机物共有4种同分异构体 | |
| C. | 乙酸和溴乙烷在一定条件下均可发生加成反应 | |
| D. | 油脂和蛋白质都属于高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
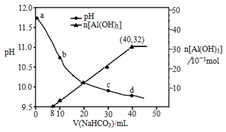 用过量烧碱溶液处理某铝土矿(含Al2O3、Fe2O3),过滤后得到滤液用NaHCO3溶液处理,测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积变化的曲线如下:下列有关说法不正确的是( )
用过量烧碱溶液处理某铝土矿(含Al2O3、Fe2O3),过滤后得到滤液用NaHCO3溶液处理,测得溶液pH和Al(OH)3生成的量随加入NaHCO3溶液体积变化的曲线如下:下列有关说法不正确的是( )| A. | V(NaHCO3)<8mL时,发生的反应为HCO3-+OH-═CO32-+H2O | |
| B. | b点与c点溶液所含微粒种类相同 | |
| C. | NaHCO3溶液的物质的量浓度为0.8 mol•L-1 | |
| D. | 生成沉淀的离子方程式为:HCO3-+AlO2-+H2O═Al(OH)3↓+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4HCO3溶于过量的浓KOH溶液中:NH4++OH-═NH3↑+H2O | |
| B. | 醋酸除去水垢:2H++CaCO3═Ca2++CO2↑+H2O | |
| C. | 向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2═2 Fe3++2Br2+6 Cl- | |
| D. | 向明矾KAl(SO4)2•12H2O]溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -═2 Al(OH)3↓+3BaSO4↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com