
【题目】同一温度下,强电解质溶液a、弱电解质溶液b、金属导体c三者的导电能力相同,若升高温度后,它们的导电能力强弱顺序是( )
A. b>a>c B. a=b=c
C. c>a>b D. b>c>a
 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:
【题目】如图所示三个烧瓶中分别装入含酚酞的0.01 mol/LCH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,向烧杯③中加入NH4NO3晶体,烧杯②中不加任何物质.
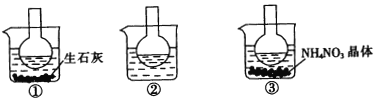
(1)含酚酞的0.01 mol/L CH3COONa溶液显浅红色,其原因为____________________.
(2)实验过程中发现烧瓶①中溶液红色变深,烧瓶③中溶液红色变浅,则下列叙述正确的是___________.
A.水解反应为放热 反应 B.水解反应为吸热反应
C.NH4NO3溶于水时放出热量 D.NH4NO3溶于水时吸收热量
(3)向三份0.01 mol L—1的CH3COONa溶液中分别加入少量浓盐酸、NaOH固体、Na2CO3固体,则CH3COO-的水解平衡分别________、_________、_________。(填向“左移动”“向右移动”或“不移动”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定平衡常数对定量认识化学反应具有重要意义。已知:I2能与 I-反应生成 I3-,并在溶液中建立如下平衡: I2+I-![]() I3-。通过测平衡体系中 c(I2)、 c(I-)和 c(I3-),就可求得该反应的平衡常数。
I3-。通过测平衡体系中 c(I2)、 c(I-)和 c(I3-),就可求得该反应的平衡常数。
Ⅰ.某同学为测定上述平衡体系中 c(I2),采用如下方法:取 V1 mL 平衡混合溶液,用cmol·L-1的Na2S2O3溶液进行滴定(反应为 I2+2Na2S2O3=2NaI+Na2S4O6),消耗 V2 mL 的Na2S2O3溶液。根据V1、V2和c可求得c(I2)。
(1)上述滴定时,可采用________做指示剂,滴定终点的现象是_____________________。
(2)下列对该同学设计方案的分析,正确的是________(填字母)。
A.方案可行。能准确测定溶液中的 c(I2)
B.不可行。因为 I-能与 Na2S2O3发生反应
C.不可行。只能测得溶液中 c(I2)与 c(I3-)之和
Ⅱ.化学兴趣小组对上述方案进行改进,拟采用下述方法来测定该反应的平衡常数(室温条件下进行,溶液体积变化忽略不计):

已知: ①I-和 I3-不溶于 CCl4; ②一定温度下, 碘单质在四氯化碳和水混合液体中,碘单质的浓度比值即![]() 是一个常数(用Kd表示,称为分配系数),且室温条件下Kd=85。回答下列问题:
是一个常数(用Kd表示,称为分配系数),且室温条件下Kd=85。回答下列问题:
(3)操作Ⅰ使用的玻璃仪器中,除烧杯、玻璃棒外,还需要的仪器是________(填名称)。试指出该操作中应注意的事项为________。 (任写一条)
(4)上述测定过程均正常操作,下层液体中碘单质的物质的量浓度是________;若终点读数时俯视滴定管, 则会造成所测浓度________ (填“等于”、 “大于”或“小于”)该值。
(5)实验测得上层溶液中 c(I3-)=0.0049 mol·L-1,结合上述有关数据,计算室温条件下反应 I2+I-![]() I3-的平衡常数 K=________(用具体数据列出计算式即可)。
I3-的平衡常数 K=________(用具体数据列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向10 mL 0.1 mol·L-1 H2A溶液中滴加等浓度的NaOH溶液,溶液的pH与NaOH溶液的体积关系如图所示。下列叙述错误的是

A. C点溶液中含有NaHA和Na2A
B. NaHA溶液中水的电离程度比Na2A溶液中小
C. B点,c (Na+)=2[c (H2A)+c (HA)+c (A2-)]
D. D点,c (Na+)>c (A2-)>c (OH-)>c (HA-)>c (H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】凤凰石是一种用于建材装饰的硅酸盐矿物,已知某地出产的凤凰石可看作由主要成分硅酸铜盐X·3H2O(摩尔质量=334g/mol)与含氧酸盐杂质Y共同组成,X、Y均含三种元素,工业上利用下列流程制备铜盐,在溶液Ⅱ中滴入KSCN溶液显血红色。

请回答:
(1)杂质Y中除氧以外还含有的元素为_____(填元素符号),x的化学式为_______。
(2)如果王溶液Ⅱ中继续加入H2O2,发现有气泡产生,有观点认为是Y中的某元素离子将H2O2氧化所导致,写出反应的离子方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有未知浓度的Ba(OH)2和NaOH混合溶液,量取四份该溶液分别通入等量的CO2(已折算成标准状况下的体积,不考虑CO2在水中的溶解),生成沉淀的物质的量如下表:
实验序号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
CO2体积(mL) | 2352 | 2352 | 2352 | 2352 |
样品体积(mL) | 20.0 | 30.0 | 40.0 | 50.0 |
沉淀物质的量(×10-2mol) | 1.50 | 4.50 | 6.00 | 7.50 |
(1)该混合溶液中Ba(OH)2的物质的量浓度=_____________。
(2)实验Ⅲ最后所得溶液中碳酸钠的物质的量=___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】废气中的H2S通过高温热分解可制取氢气:2H2S(g)![]() 2H2(g)+ S2(g)(正反应吸热)。现在3L密闭容器中,控制不同温度进行H2S分解实验。
2H2(g)+ S2(g)(正反应吸热)。现在3L密闭容器中,控制不同温度进行H2S分解实验。
(1)某温度时,测得反应体系中有气体1.31 mol,反应10 min后,测得气体为l.37 mol,则10 min 内H2的平均生成速率为________________。
(2)某温度时,判断H2S的转化率达到最大值的依据是________(选填编号)。
a.气体的压强不发生变化 b.气体的密度不发生变化
c.单位时间里分解的H2S和生成的H2一样多 d.反应物不再转化为生成物
(3)如图所示,该可逆反应在t0时因改变某外界条件而打破原平衡,在t1时达到新的平衡状态,因此推断,t0时改变的外界条件可能是__________________、___________________。

(4)在容器体积不变的情况下,如果要提高H2S的转化率,可采取的一种措施是_____________。
(5)在实验室,若将H2S通入浓硫酸中,发生的化学反应的方程式是:__________。
(6)若将H2S完全燃烧后,并用碳酸钠与碳酸氢钠的混合溶液吸收生成气体SO2,发生如下反应:2Na2CO3+SO2+H2O→ 2NaHCO3+Na2SO3
充分反应后(无CO2逸出),所得溶液组成如表:
物质 | Na2CO3 | NaHCO3 | Na2SO3 |
物质的量(mol) | 2 | 12 | 4 |
则原吸收液中碳酸钠与碳酸氢钠的物质的量之比________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是三种元素的原子,质子数都小于18。A原子与B原子的最外层电子数都是6,A原子与C原子的核外电子层数都为3, C原子的质子数比A少4。回答下列问题:
(1)A、B的元素符号分别为___________________。
(2)A的离子结构示意图为_________;A与C组成的化合物为________(用具体元素符号表示)。
(3)元素A的一种质量数为32的核素,与元素B的一种核素构成微粒为AB42-,1mol AB42-的质量为104g,则元素B的该核素中的中子数为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com