
| 元素代号 | A | B | D | E | G | H | I | J |
| 化合价 | -1 | -2 | +4、-4 | +4、-2 | +5、-3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.102 | 0.110 | 0.143 | 0.160 | 0.186 |
 .
.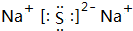 .
. 分析 短周期元素中,B、E均有-2价,处于ⅥA族,且原子半径E>D,则D为O、E为S;A有-1价,原子半径小于O,且与O原子半径相差不大,则A为F元素;D有+4、-4价,处于IV族,原子半径大于氧,且与氧原子半径相近,故D为碳元素;G有+5、-3价,原子半径大于S,故G为P;J、I、H化合价分别为+1、+2、+3,分别处于ⅠA族、ⅡA族、ⅢA族,原子半径J>I>H,且大于P原子半径,故J为Na、I为Mg、H为Al,据此解答.
解答 解:短周期元素中,B、E均有-2价,处于ⅥA族,且原子半径E>D,则D为O、E为S;A有-1价,原子半径小于O,且与O原子半径相差不大,则A为F元素;D有+4、-4价,处于IV族,原子半径大于氧,且与氧原子半径相近,故D为碳元素;G有+5、-3价,原子半径大于S,故G为P;J、I、H化合价分别为+1、+2、+3,分别处于ⅠA族、ⅡA族、ⅢA族,原子半径J>I>H,且大于P原子半径,故J为Na、I为Mg、H为Al.
(1)E为S元素,处于第三周期VIA族,故答案为:三;VIA;
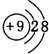
(2)电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大,故离子半径:F->Na+>Al3+,F-离子结构示意图为 ,
,
故答案为:F->Na+>Al3+; ;
;
(3)上述元素的最高价氧化物对应水化物的酸性最强的为硫酸,碱性最强的为NaOH,这两种元素形成化合物为Na2S,电子式为 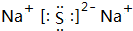 ,
,
故答案为:S;Na;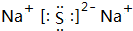 .
.
点评 本题考查结构性质位置关系应用,关键是根据化合价与原子半径推断元素,注意对元素周期律的理解掌握.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
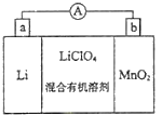 如图是锂锰电池的反应原理示意图,其中电解质KClO4溶于混合有机溶剂中,Li+ 通过电解质迁移入MnO2晶格中,得到LiMnO2.回答下列问题:
如图是锂锰电池的反应原理示意图,其中电解质KClO4溶于混合有机溶剂中,Li+ 通过电解质迁移入MnO2晶格中,得到LiMnO2.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 亚硫酸钠 | B. | 硝酸银 | C. | 碳酸钠 | D. | 氯化铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
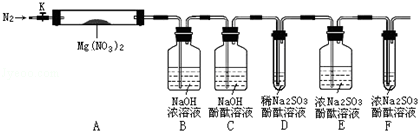
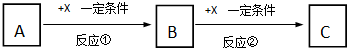
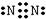 ,步骤Ⅱ中,通入一段时间N2的目的是避免对分解产物O2的检验产生干扰.
,步骤Ⅱ中,通入一段时间N2的目的是避免对分解产物O2的检验产生干扰.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com