
在可逆反应2SO2+O2 2SO3的平衡状态下,保持恒温恒容向容器中加入一定量的O2,下列说法正确的是(K为平衡常数,QC为浓度商)
2SO3的平衡状态下,保持恒温恒容向容器中加入一定量的O2,下列说法正确的是(K为平衡常数,QC为浓度商)
A.QC不变,K变大,O2转化率增大
B.QC变小,K不变,O2转化率减小
C.QC不变,K变大,SO2转化率增大
D.QC增大,K不变,SO2转化率增大
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2017届河北省高三上五调考试化学卷(解析版) 题型:填空题
工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
I.脱硝:已知:H2的热值为142.9 kJ/g(热值是表示单位质量的燃料完全燃烧时所放出的热量);
N2(g) + 2O2(g)= 2NO2(g) △H= +133 kJ/mol
H2O(g) =H2O(l) △H=- 44 kJ/mol
催化剂存在下,H2还原NO2生成水蒸气和其他无毒物质的热化学方程式为_____________。
Ⅱ.脱碳:向2L密闭容器中加入2 mol CO2、6 mol H2,在适当的催化剂作用下,发生反应 CO2(g) + 3H2(g)  CH3OH(l) + H2O(l)。
CH3OH(l) + H2O(l)。
(1)①该反应自发进行的条件是___________(填“低温”“高温”或“任意温度”)。
②下列叙述能说明此反应达到平衡状态的是___________。
A.混合气体的平均式量保持不变
B.CO2和H2的体积分数保持不变
C.CO2和H2的转化率相等
D.混合气体的密度保持不变
e.1 mol CO2生成的同时有3 mol H—H键断裂
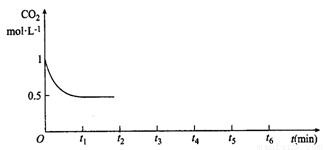
③CO2的浓度随时间(0~t2)的变化如图所示,在t2时将容器容积缩小一倍,t3时达到平衡,t4时降低温度,t5时达到平衡,请画出t2~t6的浓度随时间的变化。
(2)改变温度,使反应CO2(g)+3H2(g) CH3OH(g) + H2O(g) △H<0中的所有物质都为气态。起始温度体积相同(T1℃、2L.密闭容器)。反应过程中部分数据见下表:
CH3OH(g) + H2O(g) △H<0中的所有物质都为气态。起始温度体积相同(T1℃、2L.密闭容器)。反应过程中部分数据见下表:
反应时间 | CO2 (mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
反应I 恒温恒容 | 0 min | 2 | 6 | 0 | 0 |
10 min | 4.5 | ||||
20 min | 1 | ||||
30 min | 1 | ||||
反应II绝热恒容 | 0 min | 0 | 0 | 2 | 2 |
①达到平衡时,反应I、II对比:平衡常数K( I ) __________K(II)(填“>”“<”或“=”,下同);平衡时CH3OH的浓度c(I)___ ________c(II)。
②对反应I,前10 min内的平均反应速率v(CH3OH) =____________,在其他条件不变下,若30 min时只改变温度为T2℃,此时H2的物质的量为3.2 mol,则T1_________T2(填填“>”“<”或“=”)。若30 min时只向容器中再充入1 mol CO2(g)和1mol H2O(g),则平衡 ______________移动(填“正向”、“逆向”或“不”)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二12月月考化学卷(解析版) 题型:选择题
a、b、c、d是四种短周期元素,a、b、d同周期,c、d同主族。a的原子结构示意图为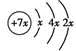 ,b与c形成化合物的电子式为
,b与c形成化合物的电子式为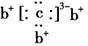 。下列比较中正确的是
。下列比较中正确的是
A. 原子半径:a>c>d>b B. 电负性:a>b>d>c
C. 原子序数:a>d>b>c D. 最高价含氧酸的酸性:c>d>a
查看答案和解析>>
科目:高中化学 来源:2017届西藏林芝一中高三上月考四化学试卷(解析版) 题型:推断题
化合物A的分子式为C9H15OCl,分子中含有一个六元环和一个甲基,环上只有一个取代基且可以发生银镜反应;F分子中不含甲基:A与其它物质之间的转化如下图所示:
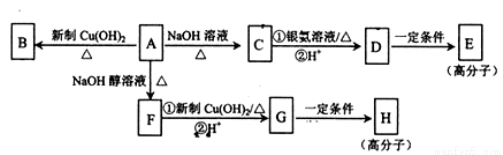
(1)A-F的反应类型是__________; G中含氧官能团的名称是_____________。
(2)A-C的反应方程式是___________。
(3)H的结构简式是______________,E的结构简式是__________。
(4)有的同学认为B中可能没有氯原子,你认为可能的原因是_____________。
(5)某烃的含氧衍生物X符合下 列条件的同分异构体中,核磁共振氢谱显示为2组峰的是________(写结构简式);只含有两个甲基的同分异构体有__________种。
列条件的同分异构体中,核磁共振氢谱显示为2组峰的是________(写结构简式);只含有两个甲基的同分异构体有__________种。
①相对分子质量比C少54;②氧原子数与C相同;③能发生水解反应。
查看答案和解析>>
科目:高中化学 来源:2017届西藏林芝一中高三上月考四化学试卷(解析版) 题型:选择题
下列离子方程式正确的是 ( )
A.向苯酚钠溶液中通入少量的CO2:C6H5O-+CO2+H2O → C6H5OH+HCO3-
B.将氯气通入水中:Cl2+H2O= Cl - + ClO-+2H+
C.向AlCl3溶液中加入过量氨水:Al3++4NH3•H2O=AlO2 -+4NH4++2H2O
D.钠与CuSO4溶液反应:2Na+Cu2+=Cu↓+2Na+
查看答案和解析>>
科目:高中化学 来源:2017届西藏拉萨中学高三上期末理综化学卷(解析版) 题型:选择题
下列有关氨或铵盐的说法不正确的是
A.可用湿润的红色石蕊试纸检验氨气
B.用盐酸滴定氨水,当溶液呈中性时,c(NH4+) = c(Cl-)
C.NH3属于弱电 解质
解质
D.常温时,0.1mol·L-1NH4Cl溶液加水稀释, 的值不变
的值不变
查看答案和解析>>
科目:高中化学 来源:2017届江西师大附中高三12月月考化学试卷(解析版) 题型:选择题
肼(N2H4)是一种可用于火箭或原电池的燃料。已知:
N2(g)+2O2(g)=2NO2(g) ΔH=+67.7 kJ·mol-1 ①
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-534 kJ·mol-1②
下列说法正确的 是( )
是( )
A.反应①中反应物所具有的总能量大于生成物所具有的总能量
B.2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g) ΔH=-1 000.3 kJ·mol-1
C.铂作电极,KOH溶液作电解质溶液,由反应②设计的燃料电池,其负极反应式为N2H4-4e-+4OH-=N2+4H2O
D.铂作电极,KOH溶液作电解质溶液,由反应②设计的燃料电池,工作一段时间后,KOH溶液的pH将增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年宁夏高二上月考二化学卷(解析版) 题型:推断题
已知: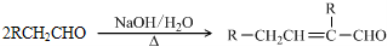
水杨酸酯E为紫外线吸收剂,可用于配制防晒霜.E的一种合成路线如下:
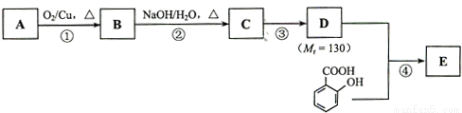
请回答下列问题:
(1)一元醇A中氧的质量分数约为21.6%;结构分析显示A只有一个甲基,A的名称为 .
(2)C有______种结构;若一次取样,检验C中所含官能团,按使用的先后顺序写出所用试剂: _ .
(3)第③步的反应类型为______________;
(4)同时符合下列条件的水杨酸同分异构体的数目:__________.
a.分子中有6个碳原子在一条直线上;
b.分子中所含官能团包括水杨 酸具有的官能团.
酸具有的官能团.
(5)写出E的结构简式: _.
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林长春外国语学校高一上月考二化学卷(解析版) 题型:选择题
A、B是两个完全相同的装置,如下图所示,某学生分别在A、B的侧管中装入1.06 g Na2CO3和0.84 g NaHCO3,A、B中分别装有10 mL相同浓度的盐酸,将两个侧管中的物质同 时倒入各自的试管中,下列叙述正确的是
时倒入各自的试管中,下列叙述正确的是
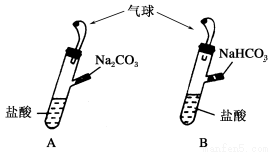
A.A装置的气球膨胀得快
B.若最终两气球体积相同,则盐 酸的浓度一定大于或等于2 mol·L-1
酸的浓度一定大于或等于2 mol·L-1
C.若最终两气球体积不同,则盐酸的浓度一定小于或等于1 mol·L-1
D.最终两试管中Na+、Cl-的物质的量一定相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com