
【题目】下列叙述错误的是
A. 常温下,pH=3的盐酸与pH=11的氨水溶液中水的电离程度相同
B. 常温下两种溶液①0.1mol/L CH3COOH溶液 ②0.3mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积的混合液,c(H+):①>②
C. 室温下向10mL pH=3的醋酸溶液中加入水稀释后溶液中c(CH3COO-)/[c(CH3COOH)·c(OH-)]不变
D. MOH和ROH两种碱的溶液分别加水稀释时,pH变化如图所示则稀释前,c(ROH)<10c(MOH)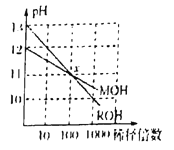
【答案】B
【解析】A、常温下,pH=3的盐酸抑制水电离,水电离的c(H+)=10-11mol·L-1,pH=11的氨水抑制水电离,水电离的c(OH-)=10-11mol·L-1,pH=3的盐酸与pH=11的氨水溶液中水的电离程度相同,故A正确;B、①0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积的混合液成为0.05mol·L-1的CH3COONa,②0.3mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积的混合液中溶质为0.1mol·L-1的CH3COOH和0.05mol·L-1的CH3COONa,醋酸的电离大于水解,所以c(H+):①<②,故B错误;C. 室温下向10mLpH=3的醋酸溶液中加入水稀释后溶液中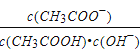 =
=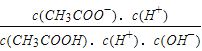 =ka/kw,温度不变,两常数的比值不变。故C正确;D、ROH为强碱,稀释前浓度为0.1mol·L-1,MOH的pH=12时稀释100倍,pH变为11,则说明MOH为弱碱,稀释前MOH的浓度大于0.01mol·L-1,则稀释前c(ROH)<10c(MOH),故D正确;故选B。
=ka/kw,温度不变,两常数的比值不变。故C正确;D、ROH为强碱,稀释前浓度为0.1mol·L-1,MOH的pH=12时稀释100倍,pH变为11,则说明MOH为弱碱,稀释前MOH的浓度大于0.01mol·L-1,则稀释前c(ROH)<10c(MOH),故D正确;故选B。


科目:高中化学 来源: 题型:
【题目】有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH4+、Cl-、Mg2+、Ba2+、CO32-、SO42-,现取三份100mL该溶液进行如下实验:(1)第一份加入AgNO3溶液有沉淀产生;(2)第二份加足最NaOH溶液加热后,收集到气体0.04 mol;(3)第三份加足量BaCl2溶液后,干燥后得到沉淀6.27g,经足量盐酸洗涤、干燥后,沉淀质量为2.33g。根据上述实验,下列推测正确的是
①K+一定存在;②100mL溶液中含0.01molCO32-;③Cl-可能存在;④ Ba2+一定不存在;⑤Mg2+可能存在
A. ②③④ B. ③④⑤ C. ①②③ D. ①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在水溶液中存在反应:Ag++Fe2+Ag(s)+Fe3++Q,达到平衡后,为使平衡体系中析出更多的银,可采取的措施是( )
A.升高温度B.加水稀释C.增大Fe2+的浓度D.常温下加压
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在反应 3 Cl2 + 6KOH = 5KCl + KClO3 + 3H2O 中,被氧化的氯原子与被还原的氯原子的质量之比是
A. 1:6 B. 6:1 C. 5:1 D. 1:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列两种物质发生反应 ①Na和O2②AlCl3与氨水 ③水玻璃与CO2④Fe与Cl2⑤Fe和稀HNO3,因反应物用量或反应条件的不同而生成不同产物的是( )
A.①②③④⑤B.①②③⑤C.①②⑤D.①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把小块木炭在酒精灯上烧至红热,迅速投入热的浓硝酸中,发生剧烈反应,同时有大量红棕色气体产生,液面上木炭迅速燃烧发出光亮.
(1)写出红热木炭被热的浓硝酸氧化为CO2的化学方程式 .
(2)木炭与浓硝酸反应过程中还伴随着浓硝酸的分解,除了产生氧气外,也产生红棕色气体.相同条件下该分解反应产生的氧气与红棕色气体的体积之比为 .
(3)某研究性学习小组的同学对“木炭在液面上迅速燃烧发出光亮”的原因做出3个猜想: 猜想一:甲同学认为空气中O2支持木炭燃烧
猜想二:乙同学认为浓硝酸分解产生的O2支持木炭燃烧
猜想三:丙同学认为反应产生的NO2支持木炭燃烧
①根据木炭在空气中燃烧的现象,甲同学的猜想明显不合理,理由是 .
②理论分析乙同学的猜想也不正确,原因是 .
③要证实丙同学的猜想,还需补充的实验方案是(请写出实验操作、现象和结论).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活密切相关,下列有关说法正确的是
A.葡萄糖注射液能产生丁达尔效应
B.高纯度的硅单质广泛用于制作光导纤维
C.二氧化硫的大量排放是造成光化学烟雾的主要原因
D.汽车的排气管上装有“催化转化器”,使有毒的CO和NO反应生成N2和CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃、101kPa下,断开1mol H2中的化学键需吸收436kJ的热量,断开1mol Cl2中的化学键需吸收243kJ的热量,断开1mol HCl分子中的化学键需吸收431kJ的热量,试求5mol H2和5mol Cl2完全反应的能量变化为kJ(填“吸收或放出”+能量数值).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com