
【题目】下列关于实验室制备乙酸乙酯和乙酸丁酯的描述正确的是
A. 均采用水浴加热 B. 均采用边反应边蒸馏的方法
C. 制备乙酸乙酯时乙醇过量 D. 制备乙酸丁酯时正丁醇过量
科目:高中化学 来源: 题型:
【题目】据报道:研究人员破解了北京及华北地区雾霾主要成分硫酸盐的形成之谜,发现在大气细颗粒物吸附的水分中NO2与SO2的化学反应是当前雾霾期间硫酸盐的主要生成路径。某实验小组对NO2和SO2的反应进行探究。
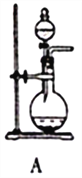
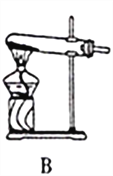
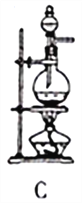

图Ⅰ 图Ⅱ
(1)SO2的发生装置可以选择图Ⅰ中的_______(填字母),反应的化学方程式为___________________。
(2)按图Ⅱ所示进行实验。
①实验时往集气瓶中通入等体积的SO2和NO2,观察到集气瓶中有白烟产生,通入的NO2气体颜色变浅,该反应的化学方程式为______________________。如果集气瓶中有少量水,则可能观察不到白烟,其原因是____________。
②请指出图Ⅱ装置设计的不合理之处___________。
(3)硫酸铵是我国pm2.5雾霾的主要成分,收集一定量的雾霾固体进行验证:
操作步骤 | 实验现象 | 结论 |
取一定量的雾霾固体于试管中,加入适量的水溶解,把溶液分成两份。 | ||
一份___________。 | 有白色沉淀生成。 | 证明雾霾固体中含有SO42- |
另一份___________。 | ___________。 | 证明雾霾固体中含有NH4+。综合上面实验,说明雾霾固体颗粒中含有(NH4)2SO4。 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表所示,提纯下列物质(括号内为杂质),所用除杂试剂和分离方法都正确的是
序号 | 不纯物 | 除杂试剂 | 分离方法 |
A | 苯中的少量苯酚 | NaOH溶液 | 分液 |
B | CH4(C2H4) | 酸性KMnO4溶液 | 洗气 |
C | 福尔马林(甲酸) | NaOH溶液 | 分液 |
D | 乙酸乙酯(乙酸) | 饱和的碳酸钠溶液 | 过滤 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标况下,将一装满NO2气体的试管倒置在水槽中,可见试管中液面逐渐上升,反应结束后,试管中所得溶液的物质的量浓度为(忽略溶质的扩散)( )
A. 1 mol/L B. 22.4 mol/L C. 0.045 mol/L D. 0.03 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,2-二溴乙烷可作抗爆剂的添加剂。如图为实验室制备1,2-二溴乙烷的装罝图, 图中分液制斗和烧瓶a中分别装有浓H2SO4和无水乙醇,d装罝试管中装有液溴。
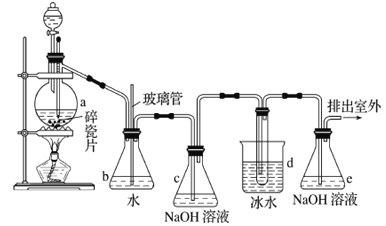
己知:CH3CH2OH![]() CH2=CH2↑+H2O;2CH3CH2OH
CH2=CH2↑+H2O;2CH3CH2OH![]() CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
相关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | 溴 | |
状态 | 无色液体 | 无色液体 | 无色液体 | 红棕色液体 |
密度/g·cm-3 | 0.79 | 2.18 | 0.71 | 3.10 |
沸点/℃ | 78.5 | 131.4 | 34.6 | 58.8 |
熔点/℃ | -114.3 | 9.79 | - 116.2 | -7.2 |
水溶性 | 混溶 | 难溶 | 微溶 | 可溶 |
(1)实验中应迅速将温度升卨到170℃左右的原因是______________________________。
(2)安全瓶b在实验中有多重作用。其一可以检查实验进行中d装罝中导管是否发生堵塞,
请写出发生堵塞时瓶b中的现象:①_______________________________;如果实验时d装罝中导管堵塞,你认为可能的原因是②_______________________________________________;安全瓶b还可以起到的作用是③__________________。
(3)容器c、e中都盛有NaOH溶液,c中NaOH溶液的作用是________________________________。
(5)除去产物中少量未反应的Br2后,还含有的主要杂质为___________,要进一步提纯,下列操作中必需的是_____________ (填字母)。
A.重结晶 B.过滤 C.萃取 D.蒸馏
(6)实验中也可以撤去d装罝中盛冰水的烧杯,改为将冷水直接加入到d装罝的试管中,则 此时冷水除了能起到冷却1,2-二溴乙烷的作用外,还可以起到的作用是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组的同学为探究原电池原理,设计如图所示装置,将锌、铜通过导线相连,置于稀硫酸中。
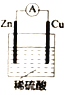
(1)锌片上的电极反应式为__________________。
(2)铜片上的现象是__________________。
(3)若反应过程中有0.2 mol电子发生转移,则生成的气体在标准状况下的体积为______________。
(4)该小组同学将稀硫酸分别换成下列试剂,电流计仍会偏转的是_________(填序号)。
A.无水乙醇 B.醋酸溶液 C.CuSO4溶液 D.苯
(5)实验后同学们经过充分讨论,认为符合某些要求的化学反应都可以通过原电池来实现。下列反应可以设计成原电池的是________(填字母代号)。
A. NaOH+HCl= NaCl+H2O B. 2H2+O2=2H2O
C. Fe+2FeCl3=3FeCl2 D. 2H2O=2H2↑+2O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计如下元素周期表,己知X元素的气态氢化物水溶液呈碱性,空格中均有对应的元素填充。以下说法正确的是
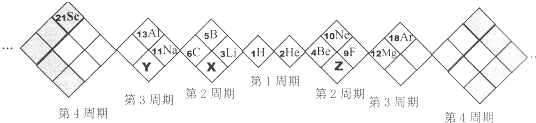
A. X、Y、Z元素分别为N、P、O
B. 白格中都是主族元素,灰格中都是副族元素
C. 原子半径:Z>X>Y
D. X、Y、Z的气态氢化物中最稳定的是:X的氢化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知在常温常压下:
①CH3CH2OH(l)+3O2(g) ═ 2CO2(g)+3H2O(g) ΔH1=-1366kJ·mol-1
②H2O(g) ═ H2O(l) ΔH2=-44kJ·mol-1
③CH3CH2OH(l)+2O2(g)═2CO(g)+3H2O(l) ΔH3=-932kJ·mol-1
写出CO燃烧热的热化学方程式 ____________。
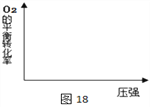
(2)在图18中画出不同温度下(T1>T2),上述反应③中O2的平衡转化率随压强变化的关系图(请在图上标注温度T1、T2)。________
(3)一定条件下,在体积为2 L的密闭容器中发生反应:CO(g) + 2H2(g)![]() CH3OH(g)达到化学平衡状态。
CH3OH(g)达到化学平衡状态。
①该反应的平衡常数表达式K=__________;根据图19判断,升高温度,平衡常数K值将_____(填“增大”、“减小”或“不变”)。

②500℃时,从反应开始至达到化学平衡,以H2的浓度变化表示的化学反应速率是____。
③X点与Y点的平均速率:v(X)____v(Y);其中X点的正反应速率v正(X)与Z点的逆反应速率v逆(Z)的大小关系为v正(X)____v逆(Z)(填“>”、“<”、“=”)。
(4)一定条件下,CO可与粉末状的氢氧化钠作用生成甲酸钠。
①已知常温时,0.1mol/L的甲酸溶液其pH约为2.4,请用离子反应方程式表示甲酸钠的水溶液呈碱性的原因_________。
②向20mL 0.1mol/L的甲酸钠溶液中小心滴加10mL 0.1mol/L的盐酸,混合液呈酸性,请按由大到小的顺序给溶液中离子浓度排序_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com