
 ��������Ҫ�Ļ�����Ʒ֮һ��
��������Ҫ�Ļ�����Ʒ֮һ��| t/�� | 200 | 300 | 400 |
| K | K1 | K2 | 0.5 |
���� ��1���������Ȼ�ѧ����ʽ����д����������д��
�����ݻ�ѧƽ��������ɰ������ʵ���������Ȼ�ѧ����ʽ����Q1������ͬ����������г���2mol N2��6molH2�����Կ�����ԭ��ƽ���м���1mol������3mol�������൱������ѹǿ��ƽ��������м��������ƽ���ų�������ΪQ2kJ��
�����ݷ�Ӧ�ʱ�=��Ӧ����ѻ�ѧ�����յ�����-�������γɻ�ѧ���ų�����������õ�N-H���������յ�������
��2���ٶ��ڷ��ȷ�Ӧ���¶�Խ�ߣ�ƽ�������ƶ�����Ӧƽ�ⳣ��ԽС��
�ڸ���ƽ��״̬���ж������жϣ�
�ۻ�ѧƽ�ⳣ��������Ӧƽ�ⳣ�����㷴Ӧ��ƽ�ⳣ����Ϊ����������Ũ���غ�ƽ�ⳣ���Ĺ�ϵ��ȷ��ƽ����ƶ�����
��� �⣺��1���ٺϳ�����ÿÿ����3mol H2���ų�92.2kJ�����������Ȼ�ѧ����ʽд������ע���ʾۼ�״̬�Ͷ�Ӧ��Ӧ�ų�������д���Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��=2NH3��g����H=-92.2kJ/mol��
�ʴ�Ϊ��N2��g��+3H2��g��=2NH3��g����H=-92.2kJ/mol��
����ͼ��N2��H2��Ӧ����2mol NH3�����������仯ʾ��ͼ����Ӧ�ʱ��H=335KJ/mol-427.2KJ/mol=-92.2KJ/mol��
N2��g��+3H2��g��=2NH3��g����H=-92.2KJ/mol
1 3 0
0.2 0.6 0.4
����0.4mol��������=$\frac{0.4mol}{2mol}$��92��2KJ=18.44KJ��
����ͬ����������г���2mol N2��6mol H2�����Կ�����ԭ��ƽ���м���1mol������3mol�������൱������ѹǿ��ƽ��������д�ƽ���ų�������Q2 ����2Q1��
�ʴ�Ϊ��18.44������
�ۺϳɰ���ҵ�У�3H2+N2?2NH3����Ӧ�ʱ�=��Ӧ����ѻ�ѧ�����յ�����-�������γɻ�ѧ���ų�������=3��436+945.8-6��N-H������=-92.2��N-H������=391kJ���ʴ�Ϊ��391��
��2���ٸ÷�Ӧ����Ӧ�Ƿ��ȷ�Ӧ�������¶ȣ�ƽ�����淴Ӧ�����ƶ���������Ũ�ȼ�С����Ӧ��Ũ����������K1��K2���ʴ�Ϊ������
��N2��g��+3H2��g��?2NH3��g����H��0����Ӧ�����������С�ķ��ȷ�Ӧ����
a�������ڸ����ʵ�Ũ��֮�ȵ��ڼ�����֮�ȣ�����֤�����淴Ӧ������ȣ���a����
b����ͬ���ʵ����淴Ӧ����֮�ȵ����������֮����ƽ��״̬��3�ԣ�N2��������=�ԣ�H2�����棩��ƽ��״̬����b����
c��������ѹǿ���䣬��������ʵ������䣬�÷�Ӧ��ƽ��״̬����c��ȷ��
d����������ܱ������з�Ӧ���������䣬������䣬�ܶ�ʼ�ղ��䣬��d����
�ʴ�Ϊ��c��
��400��ʱ����Ӧ2NH3��g��?N2��g��+3H2��g���Ļ�ѧƽ�ⳣ��K��ֵ�ͷ�ӦN2��g��+3H2��g��?2NH3��g����ƽ�ⳣ���ʵ���������K=$\frac{1}{0.5}$=2��
���������Ϊ0.5L��N2��H2��NH3�����ʵ����ֱ�Ϊ2mol��1mol��2molʱ��400��ʱ��Ũ����Qc=$\frac{{4}^{2}}{4��{2}^{3}}$=0.5��2�������v��N2������v��N2������
�ʴ�Ϊ������
���� ���⿼�鷴Ӧ�ȵļ��㡢��ѧƽ�ⳣ����Ӱ�����ء����壬��Ӧ���ʼ���ȣ���Ŀ�Ѷ��еȣ�ע�⻯ѧƽ�ⳣ����С˵����Ӧ���г̶ȣ��뷴Ӧ�����ء��뷴Ӧ�����أ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �ڢۢ� | C�� | �٢� | D�� | �ۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | B��Ũ�Ȳ��ٱ仯 | |
| B�� | ��������ѹǿ���ٱ仯 | |
| C�� | ���������ܶȲ��ٱ仯 | |
| D�� | ��������ƽ����Է����������ٸı� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢܢ� | B�� | �٢ڢۢܢ� | C�� | �ڢۢܢݢ� | D�� | �ܢݢޢߢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
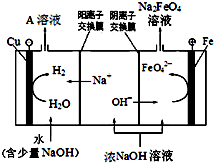 �����仯���������������о�����Ҫ�����ã�
�����仯���������������о�����Ҫ�����ã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ع���ʱ��﮵缫Ϊ������������ԭ��Ӧ | |
| B�� | ��س��ʱ��Li+�������ƶ� | |
| C�� | �õ�صĻ�ѧ�ܿ���ȫת��Ϊ���� | |
| D�� | �²��Ͼ���̼�軯�϶��ɵ�̼������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ɱ���Һ̬�Ȼ��ⶼ�ǵ���� | |
| B�� | �����Ƿ���ж����ЧӦ������ɢϵ��Ϊ��Һ����Һ�ͽ��� | |
| C�� | Na2O��Fe2O3��Al2O3�����ڼ�����������������ӻ����� | |
| D�� | Na2O2�����мȺ������Ӽ��ֺ��й��ۼ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ӧ�м������18O2���ﵽƽ���SO2�в����ܺ���18O | |
| B�� | ƽ��ʱ��SO3��Ũ�ȿ���Ϊ0.2mol/L | |
| C�� | ����������SO3ʱ��Ӧ�ﵽƽ�� | |
| D�� | �¶Ȳ��䣬�ı�SO2��O2�ļ��������ﵽƽ��ʱ$\frac{{c}^{2}��S{O}_{3}��}{{c}^{2}��S{O}_{2}����C{O}_{2}��}$���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ܣ��ۣ��ڣ��� | B�� | �ܣ��ۣ��٣��� | C�� | �ܣ��ڣ��٣��� | D�� | �ܣ��ڣ��ۣ��� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com