
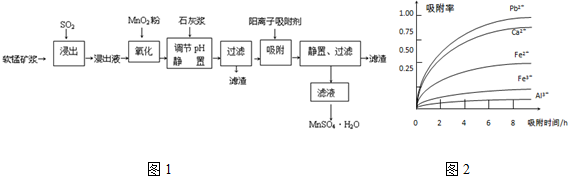
| 离子 | 离子半径(pm) | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 74 | 7.6 | 9.7 |
| Fe3+ | 64 | 2.7 | 3.7 |
| Al3+ | 50 | 3.8 | 4.7 |
| Mn2+ | 80 | 8.3 | 9.8 |
| Pb2+ | 121 | 8.0 | 8.8 |
| Ca2+ | 99 | - | - |
分析 (1)从流程图看,浸出过程是软锰矿浆(MnO2)与SO2的反应.
(2)杂质离子中只有Fe2+具有还原性,可以被MnO2在酸性条件下氧化成Fe3+;
(3)从表可以看出,只要调节pH值在4.7~8.3间,大于4.7可以将Fe3+和Al3+除去,小于8.3是防止Mn2+也沉淀;
(4)结合半径,分析右图知,图中离子从上至下,半径有减小趋势,对应的吸附率减小.随着时间的递增,所有离子的吸附率均增大;另Fe3+和Al3+离子所带电荷数大,其吸附率低;
(5)从吸附率的图可以看出,Ca2+、Pb2+的吸附率较高,
(6)电解MnSO4、ZnSO4和H4SO4的混合溶液可制备MnO2和Zn,阳极上是发生氧化反应,元素化合价升高为MnSO4失电子生成MnO2,ZnSO4反应得到电子生成Zn,结合电荷守恒书写电极反应.
解答 解:(1)低品位软锰矿浆的主要成分是MnO2,通入SO2浸出液的pH<2,其中的金属离子主要是Mn2+,则MnO2与SO2发生氧化还原反应,反应的化学方程式为SO2+MnO2=MnSO4.
故答案为:SO2+MnO2=MnSO4;
(2)杂质离子中只有Fe2+具有还原性,可以被MnO2在酸性条件下氧化成Fe3+,反应的离子方程式为2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O,
故答案为:2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O;
(3)杂质中含有Fe3+、Al3+阳离子,从图可表以看出,大于4.7可以将Fe3+和Al3+除去,小于8.3是防止Mn2+也沉淀,所以只要调节pH值在4.7~8.3间即可.
故答案为:4.7≤pH<8.3;
(4)图中离子从上至下,半径有减小趋势,对应的吸附率减小.随着时间的递增,所有离子的吸附率均增大;另Fe3+和Al3+离子所带电荷数大,其吸附率低,
故答案为:吸附时间、金属离子半径、金属离子电荷;
(5)杂质中含有Fe2+、Al3+、Ca2+、Pb2+四种阳离子,由沉淀的pH范围知,Fe2+的沉淀与Mn2+离子的沉淀所需的pH接近,而Fe3+则相差很远,故可以将Fe2+氧化成Fe3+而除杂.从吸附率的图可以看出,Ca2+、Pb2+的吸附率较高,
故答案为:Pb2+、Ca2+;
(6)电解MnSO4、ZnSO4和H2SO4的混合溶液可制备MnO2和Zn,阳极上是发生氧化反应,元素化合价升高为MnSO4失电子生成MnO2,ZnSO4反应得到电子生成Zn,阳极电极反应为:Mn2+-2e-+2H2O=MnO2↓+4H+,
故答案为:Mn2+-2e-+2H2O=MnO2↓+4H+.
点评 本题以制备硫酸锰的生产流程为知识载体,考查化学反应的书写,及除杂中的问题,题目难度中等,本题注意把握数据处理能力和图象分析能力.


科目:高中化学 来源: 题型:解答题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
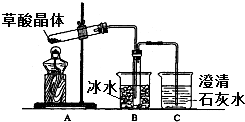 草酸(乙二酸)存在于自然界的植物中,其K1=5.4×10-2,K2=5.4×10-5.草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水.草酸晶体(H2C2O4•2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解.回答下列问题:
草酸(乙二酸)存在于自然界的植物中,其K1=5.4×10-2,K2=5.4×10-5.草酸的钠盐和钾盐易溶于水,而其钙盐难溶于水.草酸晶体(H2C2O4•2H2O)无色,熔点为101℃,易溶于水,受热脱水、升华,170℃以上分解.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
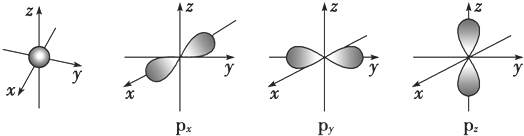
 .若元素X的原子最外层电子排布式为nsn-1npn+1,那么X的元素符号为S,原子的电子排布图为
.若元素X的原子最外层电子排布式为nsn-1npn+1,那么X的元素符号为S,原子的电子排布图为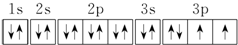 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 处理过程中银器一直保持恒重 | |
| B. | 食盐溶液作为电解质溶液形成原电池 | |
| C. | 银器为正极,Ag2S被还原生成单质银 | |
| D. | 黑色褪去的原因是黑色Ag2S转化为白色AgCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na、Mg、Al还原性依次减弱 | B. | I2、Br2、Cl2氧化性依次增强 | ||
| C. | C、N、O原子半径依次减小 | D. | P、S、Cl最高正价依次降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
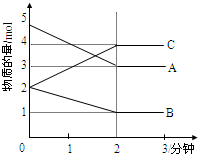 Ⅰ对于4FeS2+11O2═2Fe2O3+8SO2,试回答有关的问题:
Ⅰ对于4FeS2+11O2═2Fe2O3+8SO2,试回答有关的问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com