
【题目】在体积为2L的恒容密闭容器中发生反应![]() ,图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始
,图甲表示200℃时容器中A、B、C物质的量随时间的变化,图乙表示不同温度下平衡时C的体积分数随起始![]() :
:![]() 的变化关系。下列结论正确的是
的变化关系。下列结论正确的是![]()
![]()

A.![]() 时,反应从开始到平衡的平均速率
时,反应从开始到平衡的平均速率![]()
B.由图乙知反应![]() 的
的![]() ,且
,且![]()
C.若在图甲所示的平衡状态下,再向体系中充入0.2 mol B和0.2 mol C,重新达到平衡前![]() 正
正![]() 逆
逆![]()
D.在![]() 时,向容器中充入2 mol A和1 mol B,达到平衡时,A的体积分数大于
时,向容器中充入2 mol A和1 mol B,达到平衡时,A的体积分数大于![]()
【答案】A
【解析】
图甲可知,![]() 时平衡时,A的物质的量变化量为
时平衡时,A的物质的量变化量为![]() ,B的物质的量变化量为0.4 mol -0.2 mol =
,B的物质的量变化量为0.4 mol -0.2 mol = ![]() ,C的物质的量变化量为0.2mol,各物质变化的物质的量之比等于化学计量数之比,所以反应方程式为:2A(g)+B(g)
,C的物质的量变化量为0.2mol,各物质变化的物质的量之比等于化学计量数之比,所以反应方程式为:2A(g)+B(g)![]() C(g)。可计算平衡常数K=
C(g)。可计算平衡常数K=![]() =25。
=25。
A.由图甲可知,![]() 时5min达到平衡,平衡时B的物质的量变化量为
时5min达到平衡,平衡时B的物质的量变化量为![]() ,故
,故
![]() ,故A正确;
,故A正确;
B.在一定的温度下只要A、B起始物质的量之比刚好等于平衡化学方程式化学计量数之比,平衡时生成物C的体积分数就最大,A、B的起始物质的量之比![]() :
:![]() 。由图乙可知,
。由图乙可知,![]() :
:![]() 一定时,温度越高平衡时C的体积分数越大,说明升高温度平衡向正反应移动,升高温度平衡向吸热反应方向移动,故正反应为吸热反应,即
一定时,温度越高平衡时C的体积分数越大,说明升高温度平衡向正反应移动,升高温度平衡向吸热反应方向移动,故正反应为吸热反应,即![]() ,故B错误;
,故B错误;
C.恒温恒容条件下,再向体系中充入0.2 mol B和0.2 mol C,由于B和C的化学计量数相等,所以Qc=K,平衡不移动,故![]() ,故C错误;
,故C错误;
D.由图Ⅰ可知,![]() 时平衡时,A、B、C的物质的量变化量分别为
时平衡时,A、B、C的物质的量变化量分别为![]() 、
、![]() 、
、![]() ,物质的量之比等于化学计量数之比,故x:y:
,物质的量之比等于化学计量数之比,故x:y:![]() :
:![]() :
:![]() :1:1,平衡时A的体积分数为
:1:1,平衡时A的体积分数为![]() ,
,![]() 时,向容器中充入2molA和1molB达到平衡等效为原平衡增大压强,平衡向正反应移动,故达到平衡时,A的体积分数小于
时,向容器中充入2molA和1molB达到平衡等效为原平衡增大压强,平衡向正反应移动,故达到平衡时,A的体积分数小于![]() ,故D错误。
,故D错误。
故选A。


科目:高中化学 来源: 题型:
【题目】在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
时间(s) C(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
C(N2O4) | 0. 20 | a | 0.10 | c | d | e |
C(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅。
(1)该反应的化学方程式为__________________________,表中b_________c(填“<”、“=”、“>”)。
(2)20s时,N2O4的的浓度为__________________mol·L-1,0~20s内N2O4的平均反应速率为________________;
(3)该反应的平衡常数表达式K=___________________
在80℃时该反应的平衡常数K值为:______________(保留到小数点后2位)。
(4)在其他条件相同时,该反应的K值越大,表明建立平衡时____________。
A.N2O4的转化率越高 B.NO2的产量越大
C.N2O4与NO2的浓度之比越大 D.正反应进行的程度越大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯并(a)芘是一种致癌物、致畸源及诱变剂,也是多环芳烃中毒性最大的一种强致癌物。苯并(a)芘的结构简式如图所示,下列有关苯并(a)芘的说法中不正确的是( )
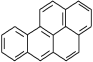
A. 苯并(a)芘的分子式为C20H12,属于稠环芳香烃
B. 苯并(a)芘与![]() 互为同分异构体
互为同分异构体
C. 苯并(a)芘在一定条件下可以发生取代反应,但不能使酸性KMnO4溶液褪色
D. 苯并(a)芘不易溶于水,易溶于苯、氯仿等有机溶剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,向0.1mol/LNaA溶液中逐滴滴加盐酸,测得混合溶液的pH与![]() 变化关系如图所示p
变化关系如图所示p![]() =-lg
=-lg![]() 。下列叙述错误的是
。下列叙述错误的是

A. E点溶液中c(Na+)=c(A-)
B. Ka(HA)的数量级为10-4
C. 滴加过程中![]() 保持不变
保持不变
D. F点溶液中c(Na+)>c(A-)>c(HA)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是![]()
A.钠与水反应:![]()
B.向![]() 溶液中通入足量氯气:
溶液中通入足量氯气:![]()
C.向AlCl3溶液中加入过量氨水:Al3++4NH3H2O=AlO2-+4NH4++2H2O
D.向碳酸氢铵溶液中加入足量石灰水:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组在实验室用三份不同初始浓度的氨基甲酸铵(NH2COONH4)溶液在不同温度下进行水解实验:NH2COONH4+2H2O![]() NH4HCO3+NH3·H2O,测得c(NH2COO-)与反应时间的关系如图所示。据图判断下列说法正确的是
NH4HCO3+NH3·H2O,测得c(NH2COO-)与反应时间的关系如图所示。据图判断下列说法正确的是
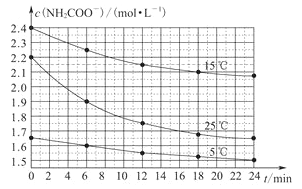
A.0~12min,初始浓度越大的实验,水解反应速率越大
B.c(NH2COO-)将随反应时间的不断延长而不断减小
C.25℃时,0~6min,v(NH2COO-)为0.05mol·L-1·min-1
D.15℃时,第30min,c(NH2COO-)为2.0mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~G是几种烃的分子球棍模型,据此回答下列问题:

(1)常温下含碳量最高的气态烃是________(填对应字母);
(2)能够发生加成反应的烃有________(填数字)种;
(3)一卤代物种类最多的是________(填对应字母);
(4)写出实验室制取C的化学方程式_______________________________________;
(5)写出F发生溴代反应的化学方程式____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用两根铂丝作电极插入KOH溶液中,再分别向两极通入甲烷气体和氧气,可形成原电池——燃料电池,该电池放电时发生的反应为CH4+2KOH+2O2===K2CO3+3H2O,下列说法错误的是( )
A. 通甲烷的一极为负极,通氧气的一极为正极
B. 放电时,通入O2一极附近溶液的pH升高
C. 放电一段时间后,KOH的物质的量不发生变化
D. 通甲烷极的电极反应式是:CH4+10OH--8e-===CO32-+7H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器中有X、Y、Z三种气体间恒温下发生的可逆反应,它们的物质的量随时间变化而变化的曲线如图所示.下列分析正确的是![]()
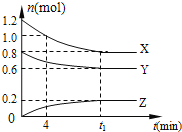
A.4min内![]()
![]()
B.Y的平衡转化率为![]()
C.平衡常数![]()
D.![]() min时充入少量He,平衡向正向移动
min时充入少量He,平衡向正向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com