
| A | 芒硝 | NaNO3 |
| B | 熟石膏 | 2CaSO4•H2O |
| C | 明矾 | KAl(SO4)2 |
| D | 绿矾 | FeCl2•7H2O |
| A. | A | B. | B | C. | C | D. | D |
分析 A.NaNO3是硝酸石的成分;
B.熟石膏是一水合二硫酸钙;
C.明矾是十二水硫酸铝钾;
D.绿矾是带7个结晶水的硫酸亚铁.
解答 解:A.芒硝是十水合硫酸钠的俗称,芒硝化学式Na2SO4•10H2O,故A错误;
B.石膏的化学式为CaSO4•2H2O,石膏[CaSO4•2H2O]加热到150~170℃时,会失去部分结晶水而生成熟石膏,熟石膏的化学式为2CaSO4•H2O,故B正确;
C.十二水硫酸铝钾的俗名为明矾,化学式为KAl(SO4)2•12H2O,故C错误;
D.绿矾是带7个结晶水的硫酸亚铁,呈浅绿色,其化学式为:FeSO4•7H2O,故D错误.
故选B.
点评 本题难度不大,熟练掌握常见化学物质的名称、俗称、化学式是正确解答此类题的关键.


科目:高中化学 来源: 题型:选择题
| A. | 任何一个水分子,其本身都是固体 | |
| B. | 逐渐加热升温,碳酸氢铵也可体现出三态变化 | |
| C. | 面包是固体,但在受压时体积缩小,故可以说固体易被压缩 | |
| D. | 在水蒸气、液态水和冰中,水分子都在不停地运动 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
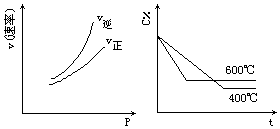 都符合图中两个图象的反应是:(C%表示某反应物的百分含量,v表示反应速率,p表示压强,t表示时间)( )
都符合图中两个图象的反应是:(C%表示某反应物的百分含量,v表示反应速率,p表示压强,t表示时间)( )| A. | N2O3(g)?NO2(g)+NO(g)-Q | B. | 3NO2(g)+H2O(l)?2HNO3 (aq)+NO(g)+Q | ||
| C. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)+Q | D. | CO2(g)+C(s)?2CO(g)-Q |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
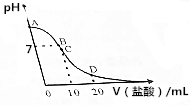 25℃,在20mL0.1mol•L-1氨水溶液中逐滴加入0.2mol•L-1HCl溶液,溶液的pH与所加盐酸的体积关系如图所示,已知0.1mol•L-1氨水的电离度为1.32%.下列说法不正确的是( )
25℃,在20mL0.1mol•L-1氨水溶液中逐滴加入0.2mol•L-1HCl溶液,溶液的pH与所加盐酸的体积关系如图所示,已知0.1mol•L-1氨水的电离度为1.32%.下列说法不正确的是( )| A. | 在A点处的溶液中pH<12 | B. | 在B点:c(NH4+)=c(Cl-)>c(OH-)>c(H+) | ||
| C. | 在C点:c(Cl-)>c(NH4+)>c(H+)>c(OH-) | D. | 在D点:c(NH4+)+c(NH3•H2O)=2c(Cl-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a<b | B. | a>b | C. | a=b | D. | 2b=a |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
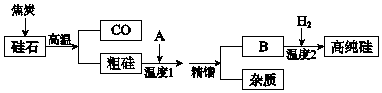
| 物质 | SiCl4 | SiHCl3 | FeCl3 | AlCl3 |
| 熔点/℃ | -70 | -128.2 | 306 | -- |
| 沸点/℃ | 57.6 | 31.85 | 315 | 181 升华 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
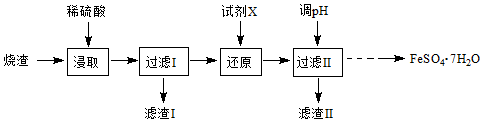
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成物能量一定低于反应物总能量 | |
| B. | 放热反应的△H>0,吸热反应的△H<0 | |
| C. | 应用盖斯定律,可计算某些难以直接测量的反应焓变 | |
| D. | 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的△H不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 废旧电池必须回收,主要目的是回收其中的金属 | |
| B. | “从沙滩到用户”,计算机芯片的材料是指单质硅 | |
| C. | 利用风能,太阳能等清洁能源代替化石燃料,可减少环境污染 | |
| D. | “光化学烟雾”,“硝酸型酸雨”的形成都与氮氧化物有关 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com