
【题目】已知,CO 的毒性表现在 CO 与血红蛋白(Hb)结合成 HbCO,使血红蛋白 失去输送 O2 功能.CO 进入血液后有如下平衡:CO+HbO2O2+HbCO,已知在人体体温37℃下,该平衡常数为 220.试回答:
(1)煤气中毒病人,可以通过进入高压氧舱的方法来救治,请用化学平衡的原理加以 说明:
(2)抽烟时,进入肺部的空气中 c(CO)=10﹣6mol/L,c(O )=10﹣2mol/L,则 c(HbCO)为 c(HbO2)的倍.
(3)已知当血液中 c(HbCO)的比值大于 0.02 时,人的智力会很快受到损伤,为避免c(HbO2 )
人的智力受到损伤,c(O2)与 c(CO)的比值应大于 .
【答案】
(1)在高压氧舱中,煤气中毒患者吸入氧气浓度较高的空气后,CO+Hb?O2?O2+Hb?CO,平衡向左移,使Hb?CO转化为Hb?O2,恢复血红蛋白的输氧功能
(2)0.022
(3)11000
【解析】解:(1)在高压氧舱中,煤气中毒患者吸入氧气浓度较高的空气后,CO+HbO2O2+HbCO,平衡向左移,使HbCO转化为HbO2,恢复血红蛋白的输氧功能,可以达到救治患者的目的,
所以答案是:在高压氧舱中,煤气中毒患者吸入氧气浓度较高的空气后,CO+HbO2O2+HbCO,平衡向左移,使HbCO转化为HbO2,恢复血红蛋白的输氧功能;
(2)因为c(CO)=10﹣6mol/L,c(O2)=10﹣2mol/L,根据 ![]() =220可知,
=220可知, ![]() =220×
=220× ![]() =0.022,
=0.022,
所以答案是:0.022;
(3) ![]() =220,
=220, ![]() >0.02,所以c(O2):c(CO)>
>0.02,所以c(O2):c(CO)> ![]() =11000,
=11000,
所以答案是:11000.
【考点精析】本题主要考查了化学平衡状态本质及特征的相关知识点,需要掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)才能正确解答此题.


 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3),又名大苏打、海波,主要用于照相业作定影剂、作鞣革时重铬酸盐的还原剂,易溶于水,遇酸易分解。其工艺制备流程如下:

某化学兴趣小组同学模拟该流程设计了如下实验装置:

回答下列问题:
(1)a处可用来检验I中的反应是否发生,选用的试剂是______________,若要停止I中的化学反应,除停止加热外,还要采取的操作是________________________。
(2)加热I,使反应完全,发现浸入液面下的铜丝变黑,甲同学对黑色生成物提出如下假设:①可能是Cu2O ②可能是CuO;③可能是CuS;④_______。乙同学提出假设①一定不成立,该同学的依据是______;丙同学做了如下实验来验证黑色物质的组成:

基于上述假设分析,黑色物质的组成为__________________________(填化学式)。
(3)II中发生反应的化学方程式为_____________________,实验中通入的SO2不能过量,可能的原因是______________________。
(4)为检验制得的硫代硫酸钠产品的纯度,该小组称取5.0g产品配成250mL硫代硫酸钠溶液,并用间接碘量法标定该溶液的浓度:向锥形瓶中加入25.00mL 0.01mol·L-1的KIO3溶液,再加入过量的KI溶液并酸化,发生反应的离子方程式为___________,再加入几滴淀粉溶液,立即用所配的Na2S2O3溶液滴定,发生反应I2 + 2S2O32- == 2I- + S4O62-,当达到滴定终点时,消耗Na2S2O3溶液20.00mL,则该产品的纯度是____________(保留3个有效数字)。
(5)丁同学提出上述实验装置的设计存在不足,建议在I上__________;在I、II之间增加_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组指定的元素不能形成AB2型化合物的是( )
A. 1s22s22p2和1s22s22p4 B. 1s22s22p63s23p4和1s22s22p4
C. 1s22s22p63s2和1s22s22p5 D. 1s22s22p5和1s22s22p4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机反应中,与其它三个反应的反应类型不同的是
A. CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
B. 2CH3COOH+Mg = (CH3COO)2Mg+H2↑
C. CH4+Cl2 ![]() CH3Cl+HCl
CH3Cl+HCl
D. ![]() +Br2
+Br2![]()
![]() +HBr
+HBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L密闭容器中,A、B、C三种物质的物质的量随时间的变化曲线如图所示。
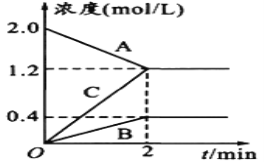
由图中数据
(1)该反应的反应物是___________。
(2)该反应是否可逆反应_____(填“是”或“否”),原因是__________________。写出该反应的化学方程式________________________。
(3)反应开始至2min,用C表示化学平均反应速率为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废水中常含有一定量的 CrO72﹣和 CrO42﹣ , 它们会对生态系统产生很大的伤害,工业上对废水处理的工艺流程如下:CrO42﹣ ![]() Cr2O72﹣→
Cr2O72﹣→ ![]() Cr3+→
Cr3+→ ![]() Cr(OH)3↓
Cr(OH)3↓
(1)CrO42﹣中 Cr 的化合价;Cr3+的核外电子排布式为 .
(2)写出第①步发生的离子反应方程式;若常温下,减 小平衡体系的 pH 至 pH=2,则溶液趋向于显色(.
(3)第②步中,还原 0.01mol Cr2O72﹣离子,需要mol 的 FeSO47H2O.
(4)已知 Cr(OH)3 在溶液中存在以下平衡:H++CrO2﹣+H2OCr(OH)3Cr3++3OH
下列有关说法中正确的是
a.加 HCl 则平衡均向右移动,则生成 Cr3+盐
b.按照物质分类 Cr(OH)3是两性氢氧化物,属于弱电解质
c.Cr3+盐中逐滴加入 NaOH 溶液,先产生沉淀,后沉淀消失
d.Cr(OH)3 饱和溶液中一定有 c(H+ )=c(OH﹣ )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4、CH3OH既是重要的化工原料,又是未来重要的能源物质。
(1)将1.0 mol CH4和2.0 mol H2O(g) 通入容积为2L的反应室,在一定条件下发生反应CH4(g)+H2O(g) ![]() CO(g)+3H2(g),测得在5 min时达到平衡,CH4的平衡转化率为40%。则0~5 min内,用H2O表示该反应的平均反应速率为_________。
CO(g)+3H2(g),测得在5 min时达到平衡,CH4的平衡转化率为40%。则0~5 min内,用H2O表示该反应的平均反应速率为_________。
(2)一定条件下,将1.0 mol CH4与2.0 mol H2O(g)充入密闭容器中发生反应CH4(g)+H2O(g) ![]() CH3OH(g)+H2(g),下列措施可以提高化学反应速率的是___________(填选项序号)。
CH3OH(g)+H2(g),下列措施可以提高化学反应速率的是___________(填选项序号)。
a.恒容条件下充入He b.增大体积
c.升高温度 d.投入更多的H2O(g)
(3)在恒容条件下进行反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),则下列实验事实可以作为判断该反应达到平衡状态标志的是___________(填选项序号)。
CH3OH(g)+H2O(g),则下列实验事实可以作为判断该反应达到平衡状态标志的是___________(填选项序号)。
a.消耗1 mol CO2同时生成1 mol CH3OH b.容器内压强保持不变
c.混合气体的密度保持不变 d.CH3OH(g)的浓度保持不变
(4)以KOH为电解质的甲醇-空气燃料电池是一种高效、轻污染的车载电池,其工作原理如图。 回答下列问题:

①该原电池的正极是____(填“甲”或“乙”),电解过程中乙电极附近pH____(填“增大”或“减小”);
②负极的电极反应式________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘在工农业生产和日常生活中有重要用途。

(1)上图为海带制碘的流程图。步骤①灼烧海带时,除需要三脚架外,还需要用到的实验仪器是____________________(从下列仪器中选出所需的仪器,用标号字母填写)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.冷凝管
步骤④发生反应的离子方程式为______________________________________________。
若步骤⑤采用裂化汽油提取碘,后果是____________________________。
(2)溴化碘(IBr)的化学性质类似于卤素单质,如能与大多数金属反应生成金属卤化物,跟水反应的方程式为:IBr+H2O==HBr+HIO,下列有关IBr的叙述中错误的是:________。
A.固体溴化碘熔沸点较高
B.在许多反应中,溴化碘是强氧化剂
C.跟卤素单质相似,跟水反应时,溴化碘既是氧化剂,又是还原剂
D.溴化碘跟NaOH溶液反应生成NaBr、NaIO和H2O
(3)为实现中国消除碘缺乏病的目标。卫生部规定食盐必须加碘盐,其中的 碘以碘酸钾(KIO3)形式存在。可以用硫酸酸化的碘化钾淀粉溶液检验加碘盐,下列说法正确的是___。
A.碘易溶于有机溶剂,可用酒精萃取碘水中的I2
B.检验加碘盐原理:IO3-+5I-+3H2O=3I2+6OH-
C.在KIO3溶液中加入几滴淀粉溶液,溶液变蓝色
D.向某无色溶液中加入氯水和四氯化碳,振荡,静置,下层呈紫色,说明原溶液中有I-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com