
【题目】25℃时,取0.lmolL-1 HA溶液与0.1 molL-1 NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因_____(用离子方程式表示)。
(2)混合溶液中由水电离出的c(OH-)___0.1 molL-1NaOH 溶液中由水电离出的c(OH-) (填“>”、“<”或“=”)。
(3)所得混合液中各离子浓度从大到小的顺序为:____。
(4)混合液中: c(HA)+ c(A-)=_______ molL-1。c(Na+)-c(A-)=_______molL-1。
(5)25℃时,已知NH4A溶液为中性,将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的 pH________7(填“>”、“<”或“=”)。
(6)相同温度下相同物质的量浓度的下列四种盐溶液,pH由大到小的顺序____(填字母)。
A.NH4HCO3 B.NH4A C.NH4HSO4 D.NH4Cl
【答案】 A- + H2O ![]() HA + OH- > c(Na+)>c(A-)>c(OH-)>c(H+) 0.05 10-6- 10-8 (或9.9×10-7) > A>B>D>C
HA + OH- > c(Na+)>c(A-)>c(OH-)>c(H+) 0.05 10-6- 10-8 (或9.9×10-7) > A>B>D>C
【解析】(1)25℃时,等体积、等浓度的HA和氢氧化钠恰好反应生成盐,测定混合溶液的pH>7,说明该溶液呈碱性,则该盐是强碱弱酸盐,酸根离子易水解;
(2)酸或碱抑制水电离,含有弱根离子的盐促进水电离;
(3)根据(1)的分析可以知道,该盐为强酸弱碱盐,溶液呈碱性,据此判断;
(4)根据元素守恒c(HA)+c(A-)=c(Na+)进行计算;根据电荷守恒计算c(Na+)-c(A-);
(5)根据题意知,HA的酸性比碳酸强,NH4A溶液为中性,说明铵根离子和该酸根离子水解程度相同,由此得知铵根离子水解程度小于碳酸根离子,所以(NH4)2CO3中溶液呈碱性;
(6)根据铵根离子的水解程度判断溶液酸碱性的大小,溶液浓度越稀,盐的水解程度越大。
详解:(1)25℃时,等体积、等浓度的HA和氢氧化钠恰好反应生成盐,测定混合溶液的pH>7,说明该溶液呈碱性,则该盐是强碱弱酸盐,酸根离子易水解,导致溶液中氢氧根离子浓度大于氢离子浓度而使溶液呈碱性,水解离子方程式为:A- + H2O ![]() HA + OH- ,
HA + OH- ,
因此,本题正确答案是:A- + H2O ![]() HA + OH- ;
HA + OH- ;
(2)酸或碱抑制水电离,含有弱根离子的盐促进水电离,NaA是含有弱根离子的盐,氢氧化钠是强碱,所以NaA促进水电离,氢氧化钠抑制水电离,则混合溶液中由水电离出的c(OH-)>0.1 molL-1NaOH溶液中由水电离出的c(OH-),
因此,本题正确答案是:>;
(3)根据(1)的分析可以知道,该盐为强酸弱碱盐,溶液呈碱性,所以离子浓度从大到小的顺序为:c(Na+)>c(A-)>c(OH-)>c(H+) ,
因此,本题正确答案是:c(Na+)>c(A-)>c(OH-)>c(H+);
(4)0.lmolL-1 HA溶液与0.1 molL-1 NaOH溶液等体积混合,所得溶液中c(Na+)=0.05mol/L,根据元素守恒 c(HA)+ c(A-)=c(Na+)=0.05mol/L,
溶液中存在电荷守恒,c(Na+)+c(H+)=c(A-)+c(OH-),所以c(Na+)-c(A-)=c(OH-)-(H+)=10-6mol/L-10-8mol/L=9.9×10-7,
因此,本题正确答案是:0.05;9.9×10-7;
(5)将HA溶液加到Na2CO3溶液中有气体放出,说明HA的酸性比碳酸的强,NH4A溶液为中性,说明相同条件下,氨水和HA的电离程度相同,所以(NH4)2CO3中铵根离子的水解程度小于碳酸根离子的水解程度,所以溶液的pH>7,
因此,本题正确答案是:>;
(6)NH4HSO4 和NH4Cl是强酸弱碱盐,铵根离子水解导致溶液呈酸性,NH4HSO4能电离出H+,所以氯化铵溶液的pH值大于硫酸铵;NH4A 溶液中阴阳离子的水解程度相等,所以溶液呈中性,溶液的pH值大于氯化铵;NH4HCO3 溶液中铵根离子的水解程度小于碳酸氢根离子的水解程度,溶液呈碱性,所以溶液的pH值最大。
因此,本题正确答案是:A>B>D>C。


科目:高中化学 来源: 题型:
【题目】利用下图装置(略去部分夹持仪器,气密性己检验)生产硷代硫酸钠晶体(Na2S2O3·5H2O)。实验步骤是先向装置①的烧瓶中滴加80%的浓H2SO4;充分反应后过滤装置③中混合物,滤液经结晶即得到产品。
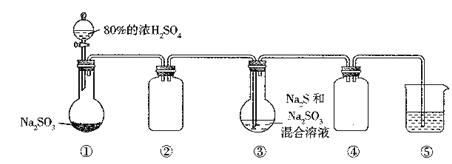
已知:2Na2S+Na2SO3+3SO2=3Na2S2O3。下列判断不正确的是
A. 应用装置①,利用H2O2和MnO2可制取少量O2
B. 实验过程中,装置②和装置④的作用相同
C. 装置③中⑤Na2S和Na2SO3的物须的量之比最好为1:2
D. 装置⑤中盛有NaOH溶液、可吸收多余的尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于“摩尔”的理解正确的是( )
A.摩尔是国际科学界建议采用的一种物理量
B.摩尔是衡量物质所含粒子数目多少的物理量
C.1mol氧含6.02×1023个O2
D.摩尔是物质的量的单位,简称摩,符号为mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
请回答下列问题:
(1)物质的量浓度相等的CH3COONa溶液和NaClO溶液pH大小关系为:c(CH3COONa)_____c(NaClO)(填“>”、“<”或“=”)。
(2)H2CO3的电离方程式为:_____。
(3)向NaClO溶液中通入少量二氧化碳气体,发生反应的离子方程式为:_____。
(4)泡沫灭火器内筒装有Al2(SO4)3溶液,外筒装有NaHCO3溶液。
① Al2(SO4)3溶液呈酸性的原因是:_____。(用离子方程式说明)
② 内、外筒溶液混合后发生反应离子方程式为:_____。
(5)常温下0.1 molL-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变大的是______。
A.c(H+) B.c(H+)·c(OH-)
C. ![]() D.
D.![]()
(6)H+浓度相等、体积相等的两份溶液A(盐酸)和B(CH3COOH)分别与锌粉反应后,仅有一份溶液中剩余锌,放出氢气的质量相同,则下列说法正确的是 __(填写序号)。
①开始反应时的速率A>B ②放出等量氢气所需要的时间B>A
③参加反应的锌的物质的量A=B ④A中有锌剩余
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在NaCl和NaBr的混合溶液中,Na+、Br-、Cl-的物质的量浓度之比不可能出现的是 ( )
A. 3:2:2 B. 5:3:2 C. 5:4:1 D. 3:2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸乙烯(CH3COOCH=CH2)是一种重要的有机化工原料,以二甲醚(CH3OCH3)与合成气(CO、H2)为原料,醋酸锂、碘甲烷等为催化剂,在高压反应釜中一步合成醋酸乙烯及醋酸。
回答下列问题:
(1)常温下,将浓度均为a mol/L的醋酸锂溶液和醋酸溶液等体积混合,测得混合液的pH=b,则混合液中c(CH3COO-)=______mol/L( 列出计算式即可)。
(2)合成二甲醚:
Ⅰ.2H2(g)+CO(g)=CH3OH(g) ΔH1=-91.8kJ/mol;
Ⅱ.2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH2=-23.5 kJ/mol;
Ⅲ.CO(g)+H2O(g)=CO2(g)+H2(g) ΔH3=-41.3 kJ/mol.
已知:H-H 的键能为436kJ/mol,C=O的键能为803kJ/mol,H-O的键能为464kJ/mol,则C≡O的键能为_____kJ/mol.
(3)二甲醚(DME)与合成气一步法合成醋酸乙烯(VAC)的反应方程式为2CH3OCH3(g)+4CO(g)+H2(g) ![]() CH3COOCH=CH2(g)+2CH3COOH(g),T℃时,向2L恒容密闭反应釜中加入0.2 molCH3OCH3、0.4 molCO、0.1molH2发生上述反应,10min达到化学平衡,测得VAC的物质的量分数为10%。
CH3COOCH=CH2(g)+2CH3COOH(g),T℃时,向2L恒容密闭反应釜中加入0.2 molCH3OCH3、0.4 molCO、0.1molH2发生上述反应,10min达到化学平衡,测得VAC的物质的量分数为10%。
①0~10min内,用CO浓度变化表示的平均反应速率v(CO)=______;该温度下,该反应的平衡常数K=__________。
②下列能说明该反应达到平衡状态的是______(填选项字母)。
A.V正(DME)=v逆(H2)≠0
B.混合气体的密度不再变化
C.混合气体的平均相对分子质量不再变化
D.c(CO):c(VAC)=4:1
③如图是反应温度对二甲醚(DME)的转化率和醋酸乙烯(VAC)选择性(醋酸乙烯的选择性Svac=![]() )的影响,该反应的ΔH______0(填“>”“<”或“=”);控制的最佳温度是___________.
)的影响,该反应的ΔH______0(填“>”“<”或“=”);控制的最佳温度是___________.

④保持温度不变,向反应釜中通入氩气增大压强,则化学平衡______(填“向正反应方向”“向逆反应方向"或“不”)移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2通入BaCl2溶液中并不产生沉淀,在下图右侧的Y形管中放置合适的药品,进行合理操作,在BaCl2溶液中可以看到白色沉淀.右侧Y形管中放的药品是( )

A. Cu和浓硝酸 B. CaO和浓氮水
C. Na2SO3和较浓硫酸 D. KMnO4溶液和浓盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是3种物质在水中的溶解度(20 ℃),下列说法中正确的是
物质 | MgCl2 | Mg(OH)2 | MgCO3 |
溶解度(g) | 54.6 | 0.000 84 | 0.039 |
A. 已知MgCO3的Ksp=2.14×10-5mol2·L-2,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)·c(CO32-)=2.14×10-5mol2·L-2
B. 除去粗盐中含有的MgCl2杂质,最佳除杂试剂为Na2CO3溶液
C. 将适量的表中的三种物质分别与足量水混合,充分加热、灼烧,最终的固体产物相同
D. 用石灰水处理水中的Mg2+和HCO3-,发生的离子反应方程式为Mg2++2HCO3-+Ca2++2OH-===CaCO3↓+MgCO3↓+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W的原子半径依次增大,X是短周期元素中原子半径最小的,Z、W同主族,且Z、W的原子序数之差与Y的原子序数相同,X、Y、Z、W的最外层电子数之和为15。下列说法正确的是( )
A. Z单质与WYZ在高温条件下反应生成W单质,说明非金属性:Z>W
B. 向无色的X2Z2Y4溶液中滴加少量酸性高锰酸钾溶液,溶液仍为无色,体现了X2Z2Y4的还原性
C. Y、Z、W的简单氢化物的稳定性依次增强
D. 由X、Y两种元素形成的所冇化合物中所含化学键的类型完全相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com