
某原电池的总反应为:Cu + 2Fe3+ = Cu2+ + 2Fe2+
A | B | C | D | |
电极材料 | Cu、Zn | Cu、Ag | Fe、Zn | Cu、C |
插入溶液 | FeCl3 | Fe(NO3) 2 | CuSO4 | Fe2(SO4)3 |
 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源:2014-2015安徽省濉溪县高一上学期期末考试化学试卷(解析版) 题型:选择题
下列离子在溶液中能大量共存的是
A.Na+、CO32—、SO42—、H+
B.K+、[Al(OH)4]—、H+、Cl—
C.Fe2+、K+、H+、NO3—
D.Al3+、H+、NO3—、SO42—
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省漳州市高三3月质量检查化学试卷(解析版) 题型:填空题
(A)【化学—物质结构与性质】(13分)
物质中铁含量的测定方法是多种多样的。
I.土壤中铁含量的测定是先将Fe3+还原为Fe2+,然后使Fe3+与邻啡罗啉 结合显橙红色,再用比色法测定。其中涉及以下反应:4FeCl3 + 2NH2OH·HCl=4FeCl2 + N2O↑+ 6HCI + H2O。
结合显橙红色,再用比色法测定。其中涉及以下反应:4FeCl3 + 2NH2OH·HCl=4FeCl2 + N2O↑+ 6HCI + H2O。
(1)基态Fe2+的核外电子排布式为 。
(2)羟胺(NH2OH)中采用sp3杂化的原子是 ;羟胺极易溶于水,主要原因是 。
(3)羟胺的组成各元素中,元素的第一电离能(I1)由大到小的顺序为 (用元素符号表示)。
(4)吡啶 和邻啡罗啉都是含氮的有机物,l mol吡啶中含有σ键的物质的量为 mol。
和邻啡罗啉都是含氮的有机物,l mol吡啶中含有σ键的物质的量为 mol。
Ⅱ.奶粉中铁含量的测定是在酸性介质中使Fe3+与K4Fe(CN)6生成普鲁士蓝(Ⅱ)(化学式为Fe4[Fe(CN)6]3),再用光度法测定铁的含量。反应原理如下:
3K4Fe(CN)6+4FeCl3=Fe4[Fe(CN)6]3↓+12KCl
(5)Fe4[Fe(CN)6]3是一种配合物,其中含有的化学键有_______;
a.共价键
b.氢键
c.配位键
d.金属键
e.离子键
(6)若K4 Fe(CN)6和FeCl3的物质的量按某种比例发生反应,可生成普鲁士蓝(I),其晶胞结构如下图所示:据此判断普鲁士蓝(I)中n(K+):n(Fe3+):n (Fe2+):n (CN—)= 。

查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省漳州市高三3月质量检查化学试卷(解析版) 题型:选择题
下列对化学知识的认识正确的是
A.H2与T2互为同位素 B.氯化铵、氯化银都属于强电解质
C.离子化合物中一定不含共价键 D.SO2、CO均属于酸性氧化物
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省邢台市高二上学期期末考试化学试卷(解析版) 题型:填空题
(12分)氢气是一种新型的绿色能源,又是一种重要的化工原料。
(1)氢气的燃烧热值高,H2(g) +1/2 O2 (g) = H2O (g) △H = -241.8 kJ·mol-1
化学键 | H-H | O=O | O-H |
键能(kJ·mol-1) | X | 496.4 | 463 |
请根据相关数据计算:H-H的键能X = ________kJ·mol-1。
(2)根据现代工业技术可以用H和CO反应来生产燃料甲醇,其反应方程式如下:
CO2 (g) + H2(g) = H2O + CH3OH(g) △H = -49.00 kJ·mol-1
一定温度下,在体积为1 L的密闭容器中充入1.00 mol CO2和3.00 mol H2,测得CO2和CH3OH的浓度随时间变化如图所示。
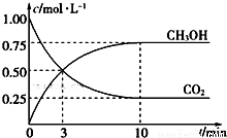
①能说明该反应已达平衡状态的是________(填代号)。
A.CO2在混合气体中的体积分数保持不变
B.单位时间内每消耗1.2 mol H2,同时生成0.4 mol H2O
C.混合气体平均相对分子质量不随时间的变化而变化
D.反应中H2O与CH3OH的物质的量浓度比为1:1,且保持不变
②从反应开始到平衡的平均反应速率v(H2) = ________,达到平衡时氢气的转化率为________。
③该温度下的平衡常数为________(小数点后保留2位)。
④下列的条件一定能加快反应速率并且提高H2转化率的是________(填代号)。
A.升高反应温度
B.缩小容器的体积
C.保持容器体积不变,充入稀有气体
D.保持容器体积不变,充入CO2气体
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省邢台市高二上学期期末考试化学试卷(解析版) 题型:选择题
CO(g) + H2O(g) = H2(g) + CO2(g) △H < 0 在其他条件不变的情况下,下列说法正确的是
A.加入催化剂,改变了反应的途径,反应的△H也随之改变
B.升高温度,逆反应速率加快,正反应速率减慢
C.升高温度,正、逆反应速率都加快,反应放出的热量不变
D.改变压强,平衡不发生移动,反应放出的热量不变
查看答案和解析>>
科目:高中化学 来源:2014-2015河北省邢台市高二上学期期末考试化学试卷(解析版) 题型:选择题
已知反应X + Y = M + N为吸热反应,对这个反应的下列说法中正确的是
A.X和Y的总能量一定低于M和N的总能量
B.因为该反应是吸热反应,故一定要加热反应才能进行
C.X的能量一定低于M的能量,Y的能量一定低于N的能量
D.破坏反应物中的化学键所吸收的能量小于形成生成物化学键所放出的能量
查看答案和解析>>
科目:高中化学 来源:2014-2015甘肃省静宁县高一上学期期末考试化学试卷(解析版) 题型:选择题
氧化还原反应的实质是
A.化合价的升降 B.分子中各原子重新组合
C.电子的得失或偏移 D.氧原子的得失
查看答案和解析>>
科目:高中化学 来源:2014-2015安徽省滁州市六校上高一联考化学试卷(解析版) 题型:填空题
(4分)对于混合物的分离或提纯,常采用的方法有:①过滤、②蒸发、③蒸馏、④萃取、⑤加热分解等。下列各组混和物的分离或提纯应采用什么方法?(填序号)
(1)提取碘水中的碘 ___________
(2)除去食盐溶液中的水 ___________
(3)淡化海水
(4)KCl中含有KClO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com