
| A. | 8个 | B. | 7个 | C. | 6个 | D. | 5个 |
分析 ①氯气和烧碱、石灰乳都能生成次氯酸盐,次氯酸盐具有强氧化性;
②氯水中含有次氯酸,次氯酸不稳定见光易分解生成氯化氢和氧气;
③食盐中的碘以碘酸钾的形式存在,只有单质碘才能与淀粉发生显色反应;
④正常雨水的PH=5.6,酸雨的PH值小于5.6;
⑤室温下,浓硫酸与铜片不反应;
⑥氯气易液化,液氯中不含氢离子,导致不和铁反应,所以可以保存在钢瓶中;
⑦常温下,浓硫酸和铝发生钝化现象;
⑧分解高锰酸钾制氧气后,残留在试管内壁上的黑色物质是二氧化锰,二氧化锰能和浓盐酸反应但不和稀盐酸反应;
⑨蒸干AlCl3溶液可得氢氧化铝;
⑩纯碱水解呈碱性.
解答 解:①氯气和烧碱、石灰乳都能生成次氯酸盐,次氯酸盐具有强氧化性,能杀菌消毒,故正确;
②氯水中含有次氯酸,次氯酸不稳定见光易分解生成氯化氢和氧气,所以逸出的气体是氧气,而不是氯气,故错误;
③食盐中的碘以碘酸钾的形式存在,只有单质碘才能与淀粉发生显色反应,故C错误;
④正常雨水的PH=5.6,酸雨的PH值小于5.6,故错误;
⑤室温下,浓硫酸与铜片不反应,加热才发生化学反应,故错误;
⑥氯气易液化,液氯中不含氢离子,导致不和铁反应,所以可以保存在钢瓶中,故正确;
⑦常温下,浓硫酸和铝发生钝化现象,所以浓硫酸可以用铝制容器盛放,故正确;
⑧分解高锰酸钾制氧气后,残留在试管内壁上的黑色物质是二氧化锰,二氧化锰能和浓盐酸反应但不和稀盐酸反应,所以不能用稀盐酸洗涤,故错误;
⑨蒸干AlCl3溶液可得氢氧化铝,而不是氯化铝,故错误;
⑩纯碱水解呈碱性,不能确定是否含有NaOH,故错误;
故选B.
点评 本题考查物质的性质,综合考查元素化合物知识,为高频考点,把握物质的性质及发生的化学反应为解答的关键,注意性质及用途的关系,题目难度不大.


 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | NH4F溶液不能存放于玻璃试剂瓶中 | |
| B. | 氮元素的非金属性强于磷,在常温下氮气活泼性也强于磷 | |
| C. | 苯不能使酸性高锰酸钾溶液褪色,所以苯不能发生氧化反应 | |
| D. | 二氧化硫和次氯酸的漂白原理不同,二氧化硫漂白时没有发生化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C和E的单质常温下不能相互反应 | |
| B. | C与B形成的两种化合物均属于离子化合物,且化学键类型完全相同 | |
| C. | 原子半径:C>D>A>B | |
| D. | A、D、E的最高价氧化物对应水化物均为弱酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
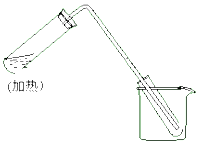 如图是用自来水制取少量蒸馏水的简易装置,(加热及固定仪器略),其原理与教材中实验完全相同.回答下列问题:
如图是用自来水制取少量蒸馏水的简易装置,(加热及固定仪器略),其原理与教材中实验完全相同.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 X、Y、Z是中学常见的三种单质,M、N是中学常见的两种化合物,其中M在常温下为液态,它们之间存在如图转化关系.下列有关说法错误的是( )
X、Y、Z是中学常见的三种单质,M、N是中学常见的两种化合物,其中M在常温下为液态,它们之间存在如图转化关系.下列有关说法错误的是( )| A. | 该过程所涉及的反应均为氧化还原反应 | |
| B. | 当X单质为金属时,可能是Na或Fe | |
| C. | 当X单质为非金属时,可能是F2或 C | |
| D. | 反应①可能在常温下进行,也可能需要在高温下才能发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | .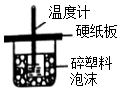 装置用于中和热的测定 | |
| B. | 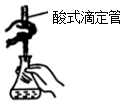 装置用于高锰酸钾溶液滴定草酸 | |
| C. | 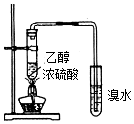 装置用于制取乙烯并验证乙烯的性质 | |
| D. | 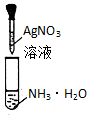 装置用于配制银氨溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ag+、Na+、Cl-、K+ | B. | Na+、Fe2+、SO42-、NO3- | ||
| C. | Mg2+、Na+、SO42-、Cl- | D. | Ba2+、HCO3-、NO3-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
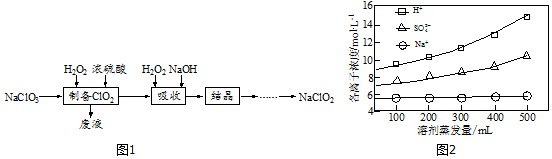
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com