

 CO2
CO2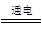 Mg+Cl2↑
Mg+Cl2↑

科目:高中化学 来源:不详 题型:单选题
| A.相同条件下,产生气体的体积相等 |
| B.生成的铝的化合物的物质的量相等 |
| C.消耗酸和碱的物质的量相等 |
| D.相同条件下,转移的电子数相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氢铝化合物与水反应生成氢氧化铝和氢气 |
| B.氢铝化合物中铝显+3价,氢显-1价 |
| C.铝与水蒸气在高温下反应可生成氢铝化合物 |
| D.氢铝化合物具有强还原性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥 |
| B.用过量氨水除去Fe3+溶液中的少量Al3+ |
| C.用新制的生石灰,通过加热蒸馏,以除去乙醇中的少量水 |
| D.Al(OH)3中混有少量Mg(OH)2:加入足量烧碱溶液,充分反应,过滤,向滤液中通入过量CO2后过滤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3 mol·L-1 HCl溶液 | B.4 mol·L-1 HNO3溶液 |
| C.8 mol·L-1 NaOH溶液 | D.18 mol·L-1 H2SO4溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


| A.b曲线表示的是向X溶液中加入NaOH溶液 |
| B.在O点时两方案中所得溶液浓度相等 |
| C.a、b曲线表示的反应都是非氧化还原反应 |
| D.X溶液显酸性,Y溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
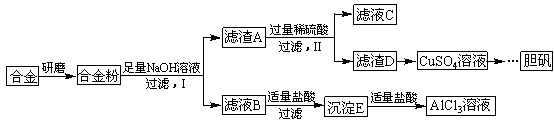
 2CuO,CuO+H2SO4=CuSO4+H2O
2CuO,CuO+H2SO4=CuSO4+H2O CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.(1)(2)(3)(4) | B.(1)(2)(4)(3) | C.(2)(3)(4)(1) | D.(3)(1)(4)(2) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
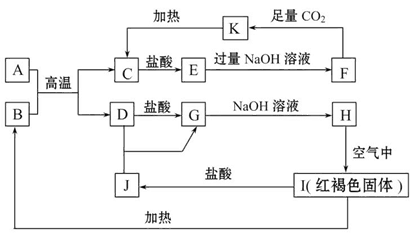
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com