
分析 根据氧化剂的氧化性强于氧化产物的氧化性判断;含有元素化合价降低的反应物为氧化剂,还原剂通过氧化反应生成的物质是氧化产物.
解答 解:(1)反应B2++D═D2++B中D元素的化合价升高,D是还原剂,B是还原产物,所以还原性是D>B;
(2)反应D2++C═C2++D中C元素的化合价升高,C是还原剂,D是还原产物,所以还原性是C>D;
(3)反应2A++B═2A+B2+,中B元素的化合价升高,B是还原剂,A是还原产物,所以还原性是B>A;
所以还原性顺序是:C>D>B>A,故答案为:还原;ABDC.
点评 本题考查根据方程式来比较氧化性和还原性强弱,难度中等,解题的关键是根据化合价找出氧化剂、还原剂、氧化产物和还原产物.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al2(SO4)3═3Al3++2SO42- | B. | AlCl3═Al3++Cl3- | ||
| C. | Mg(NO3)2═Mg2++2NO3- | D. | KMnO4═K++Mn2++4O2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向含有酚酞的NaOH溶液中通入Cl2,红色褪去,因为氯气有漂白性 | |
| B. | 液氯和氯水中都含有氯离子,滴加AgNO3溶液都产生白色沉淀 | |
| C. | 用稀盐酸可以清洗掉试管内壁上高锰酸钾分解后的黑色残留物 | |
| D. | 漂白粉漏置在空气中变质时,既有非氧化还原反应、又有氧化还原反应发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,11.2L氯气含有的分子数为0.5NA | |
| B. | 常温常压下,32gO2和O3的混合气体所含原子数为2NA | |
| C. | 1mol/L CuSO4溶液中含有NA个SO42- | |
| D. | 在电解水实验中,每生成1molH2,就有4NA个电子发生转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
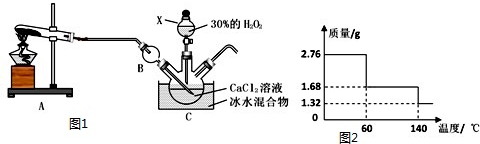
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
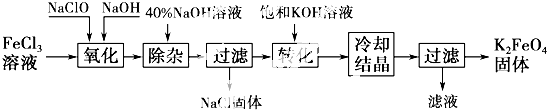
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上冶炼钠,是通过电解氯化钠饱和溶液 | |
| B. | 工业上冶炼铝,如果以石墨为电极,则阳极石墨需要不断补充 | |
| C. | 工业上冶炼镁,是电解熔融氧化镁 | |
| D. | 工业上精炼铜是粗铜为阴极 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com