
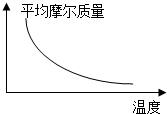
 可逆反应2A+B?2C(g)(正反应放热),随温度变化气体平均摩尔质量如图所示,则下列叙述正确的是( )
可逆反应2A+B?2C(g)(正反应放热),随温度变化气体平均摩尔质量如图所示,则下列叙述正确的是( )| A. | A和B可能都是固体 | B. | A和B一定都是气体 | ||
| C. | 若B为固体,则A一定是气体 | D. | A和B不可能都是气体 |
分析 由图可知,温度升高气体的平均相对分子质量减小,该反应正反应是放热反应,升高温度平衡向逆反应移动,据此结合物质的状态进行判断.
解答 解:A.若A和B都是固体,只有C是气体,气体的相对分子质量不变,故A错误;
B.若A为气体、B为非气体,升高温度,平衡向逆反应移动,混合气体的质量减少,混合气体的物质的量不变,混合气体平均相对分子质量减小,故A和B不一定都是气体,故B错误;
C.B为固体,A若为非气体,只有C是气体,气体的相对分子质量不变,A为气体,升高温度,平衡向逆反应移动,混合气体的质量减少,混合气体的物质的量不变,混合气体平均相对分子质量减小,故C正确;
D.若A和B都是液体,只有C是气体,气体的相对分子质量不变,故D错误;
故选C.
点评 本题考查化学平衡的影响因素,题目难度中等,注意A和B都是非气体时,只有C是气体,气体的相对分子质量不变.


 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:选择题

| A. | 该反应是复分解反应 | |
| B. | 该反应的化学方程式为Cl2+2NaClO2═2ClO2+2NaCl | |
| C. | 反应中Cl2既是氧化剂,又是还原剂 | |
| D. | 生成2 mol ClO2时转移的电子数为6 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 篮烷的分子式为C12H20 | |
| B. | 篮烷分子中存在2个六元环 | |
| C. | 篮烷分子中存在3个五元环 | |
| D. | 篮烷的一氯代物共有4种同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 5种 | C. | 6种 | D. | 8种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加催化剂 | B. | 降低温度 | C. | 减小压强 | D. | 加入O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com