
”¾ĢāÄæ”æŌŚŅ»¶ØĪĀ¶ČĻĀ£¬½«ĘųĢåXÓėĘųĢåYø÷0.16mol³äČė10LŗćČŻĆܱÕČŻĘ÷ÖŠ£¬·¢Éś·“Ó¦£ŗX£Øg£©+Y£Øg£©2Z£Øg£©”÷H£¼0£¬Ņ»¶ĪŹ±¼äŗó“ļµ½Ę½ŗā£®·“Ó¦¹ż³ĢÖŠ²ā¶ØµÄŹż¾ŻČē±ķ£ŗĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
tØMmin | 2 | 4 | 7 | 9 |
n£ØY£©ØMmol | 0.12 | 0.11 | 0.10 | 0.10 |
A.·“Ó¦Ē°4minµÄĘ½¾ł·“Ó¦ĖŁĀŹ¦Ō£ØZ£©=0.0125 molL©1min©1
B.ĘäĖūĢõ¼ž²»±ä£¬½µµĶĪĀ¶Č£¬·“Ó¦“ļµ½ŠĀĘ½ŗāĒ°¦Ō£ØÄę£©£¾¦Ō£ØÕż£©
C.øĆĪĀ¶ČĻĀ“Ė·“Ó¦µÄĘ½ŗā³£ŹżK=1.44
D.ĘäĖūĢõ¼ž²»±ä£¬ŌŁ³äČė0.2molZ£¬“ļĘ½ŗāŹ±XµÄĢå»ż·ÖŹżŌö“ó
”¾“š°ø”æC
”¾½āĪö”æ½ā£ŗA”¢ÓɱķÖŠŹż¾ŻæÉĒóµĆĒ°4minÄŚÉś³ÉZĪŖ0.10mol£¬¹Źv£ØZ£©= ![]() =0.025mol/£ØLmin£©£¬¹ŹA“ķĪó£»
=0.025mol/£ØLmin£©£¬¹ŹA“ķĪó£»
B£®ĘäĖūĢõ¼ž²»±ä£¬½µµĶĪĀ¶Č£¬Ę½ŗāÕżĻņŅʶÆŌņÕż·“Ó¦ĖŁĀŹ“óÓŚÄę·“Ó¦ĖŁĀŹ£¬¹ŹB“ķĪó£»
C£®ÓɱķÖŠŹż¾ŻæÉÖŖ7minŹ±£¬·“Ó¦µ½“ļĘ½ŗā£¬YµÄĪļÖŹµÄĮæĪŖ0.10mol£¬“ĖŹ±XµÄĪļÖŹµÄĮæŅ²ĪŖ0.10mol£¬ZµÄĪļÖŹµÄĮæŅ²ĪŖ0.12mol£¬X”¢Y”¢ZµÄĪļÖŹµÄĮæÅØ¶Č·Ö±šĪŖ£ŗ0.01molL©1”¢0.01molL©1”¢0.012molL©1£¬¹ŹĘ½ŗā³£ŹżK= ![]() =
= ![]() =1.44£¬¹ŹCÕżČ·£»
=1.44£¬¹ŹCÕżČ·£»
D£®ŅņøĆ·“Ó¦Ē°ŗóĘųĢåµÄĢå»ż²»±ä£¬ĘäĖūĢõ¼ž²»±ä£¬ŌŁ³äČė0.2 mol Z£¬Ę½ŗāµČŠ§£¬XµÄĢå»ż·ÖŹż²»±ä£¬¹ŹD“ķĪó£®
¹ŹŃ”C£®
A.4minÄŚYĪļÖŹµÄĮæ±ä»ÆĪŖ0.16mol©0.11mol=0.05mol£¬Ēó³öZµÄĪļÖŹµÄĮæ±ä»Æ£¬øł¾Żv= ![]() ¼ĘĖćv£ØZ£©£»
¼ĘĖćv£ØZ£©£»
B£®øł¾ŻĪĀ¶Č¶ŌĘ½ŗāŅĘ¶ÆµÄÓ°Ļģ·ÖĪö£»
C£®ÓɱķÖŠŹż¾ŻæÉÖŖ7minŹ±£¬·“Ó¦µ½“ļĘ½ŗā£¬øł¾ŻĘ½ŗāŹ±YµÄĪļÖŹµÄĮ棬ĄūÓĆČż¶ĪŹ½¼ĘĖćĘ½ŗāŹ±ĘäĖü×é·ÖµÄĪļÖŹµÄĮ棬ÓÉÓŚ·“Ó¦ĘųĢåĒāĘųµÄ»Æѧ¼ĘĮæŹżĻąµČ£¬ÓĆĪļÖŹµÄĮæ“śĢęÅØ¶Č“śČėĘ½ŗā³£Źż±ķ“ļŹ½¼ĘĖć£»
D£®ŌŁĶØČė0.2 mol Z£¬µČŠ§ĪŖŌŚŌĘ½ŗā»ł“”ÉĻŌö“óŃ¹Ē棬·“Ó¦Ē°ŗóĘųĢåµÄĢå»ż²»±ä£¬Ę½ŗā²»ŅĘ¶Æ£®


 ĘŚÄ©1¾ķĖŲÖŹ½Ģӿʥ¹Ą¾ķĻµĮŠ“š°ø
ĘŚÄ©1¾ķĖŲÖŹ½Ģӿʥ¹Ą¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĒč»ÆÄĘ»ÆѧŹ½ĪŖNaCN£ØCŌŖĖŲ+2¼Ū£¬NŌŖĖŲ-3¼Ū£©£¬Ēč»ÆÄĘŹĒŅ»ÖÖ°×É«½į¾§æÅĮ££¬¾ē¶¾£¬Ņ×ČÜÓŚĖ®£¬Ė®ČÜŅŗ³Ź¼īŠŌ£¬Ņ×Ė®½āÉś³ÉĒč»ÆĒā”£
£Ø1£©NaCNÓĆĖ«ŃõĖ®“¦Ąķŗ󣬲śÉśŅ»ÖÖĖįŹ½ŃĪŗĶŅ»ÖÖÄÜŹ¹ŹŖČóŗģÉ«ŹÆČļŹŌÖ½±äĄ¶µÄĘųĢ壬øĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ____________________________________________”£
£Ø2£©Ēč»ÆÄĘÓėĮņ“śĮņĖįÄʵķ“Ó¦ĪŖ£ŗNaCN+Na2S2O3ØTNaSCN+Na2SO3£»ŅŃÖŖ£ŗNaSCNÖŠSĪŖ-2¼Ū£¬Š“³öSCN-µÄµē×ÓŹ½___________”£
£Ø3£©CN-ÖŠCŌŖĖŲĻŌ£«2¼Ū£¬NŌŖĖŲĻŌ-3¼Ū£¬ĖµĆ÷·Ē½šŹōŠŌN>C£¬ĒėÉč¼ĘŹµŃéÖ¤Ć÷£ŗ_____________”£
£Ø4£©Ķ¬Ź±HCNÓÖÄÜÓėĖ®»„ČÜ£¬Ōģ³ÉĖ®ĪŪČ¾”£ŅŃÖŖ²æ·ÖČõĖįµÄµēĄėĘ½ŗā³£ŹżČē±ķ£ŗ
ČõĖį | HCOOH | HCN | H2CO3 |
µēĄėĘ½ŗā³£Źż(25”ę) | Ka=1.77”Į10-4 | Ka=5.0”Į10-10 | Ka1=4.3”Į10-7 Ka2=5.6”Į10-11 |
¢ŁĻņNaCNČÜŅŗÖŠĶØČėÉŁĮæCO2£¬·¢ÉśµÄĄė×Ó·“Ó¦ĪŖ_______________________________”£
¢ŚµČĢå»ż”¢µČĪļÖŹµÄĮæÅØ¶ČµÄHCOONaŗĶNaCNČÜŅŗÖŠĖłŗ¬Ąė×Ó×ÜŹżµÄ¹ŲĻµŹĒ£ŗHCOONa______NaCN”££ØĢī”°£¾”±”¢”°£¼”±»ņ”°=”±£©
£Ø5£©³£ĪĀĻĀ£¬ÓĆ0.10mol”¤L-1NaOHČÜŅŗ·Ö±šµĪ¶Ø20.00 mLÅØ¶Č¾łĪŖ0.10 mol”¤L-1CH3COOHČÜŅŗŗĶHCNČÜŅŗĖłµĆµĪ¶ØĒśĻßČēĻĀĶ¼”£

¢Ł³£ĪĀŹ±“×ĖįµÄµēĄė³£ŹżĪŖ1.96”Į10-5£¬0.10 mol”¤L-1CH3COOHČÜŅŗÖŠc(H+)=__________mol”¤L-1”£
¢ŚŌŚ¢ŁĖłŹ¾µÄČÜŅŗÖŠČÜÖŹĪŖ_____
¢ŪŌŚ¢ŁŗĶ¢ŚĖłŹ¾ČÜŅŗÖŠc(CH3COO-)-c(CN-)_______£ØĢī”°£¾”±”¢”°£¼”±»ņ”°=”±£©c(HCN)-c(CH3COOH)”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æCuClŹĒÉś²śÓ”Ė¢ŃÕĮĻĢŖŻ¼Ą¶µÄÖŲŅŖŌĮĻ£¬¹¤ŅµÉĻæÉÓĆŅ»ÖÖµĶĘ·Ī»Ķæó(Ö÷ŅŖ³É·ÖCuS”¢Cu2S”¢CuO”¢Fe2O3”¢FeO¼°ĘäĖū·ĒĖįČÜŠŌŌÓÖŹ)ŗĶČķĆĢæó(Ö÷ŅŖ³É·ÖĪŖMnO2ŗĶĘäĖū·ĒĖįČÜŠŌŌÓÖŹ)Ą“½ųŠŠÉś²ś£¬¹ż³ĢČēĻĀ£ŗ

»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©²½Öč¢ńÖŠ·“Ó¦½Ļ¶ą£¬ĻĀĮŠ·“Ó¦ŹĒĘäÖŠÖ®Ņ»£ŗCu2S+2MnO2+4H2SO4=2CuSO4+2MnSO4+4H2O+S£¬øĆ·“Ó¦µÄŃõ»Æ²śĪļĪŖ____________________(Ģī»ÆѧŹ½)”£
£Ø2£©ĪŖČ·¶ØĀĖŅŗ1ÖŠŹĒ·ńŗ¬ÓŠFe2+£¬Ź×ĻČÓĆÓŠ»śŻĶČ”¼Į³żČ„ČÜŅŗÖŠMnSO4£¬ŌŁČ”ĻĀ²ćĖ®ČÜŅŗ½ųŠŠ¼ģ²ā£¬ĖłÓĆŹŌ¼ĮĪŖ_____________________”£
£Ø3£©²½Öč¢ņ¼ÓČė°±Ė®æŲÖĘČÜŅŗµÄpHĪŖ5×óÓŅ£¬ÄæµÄŹĒ______________________”£
£Ø4£©ĪŖÄ£Äā²½Öč¢óµÄÉś²ś¹ż³Ģ£¬Ä³Ķ¬Ń§Éč¼ĘČēĻĀŹµŃ飬ĻĀĮŠÓŠ¹ŲŠšŹöÕżČ·µÄŹĒ_____________”£

A.aĶØČėCO2£¬Č»ŗóbĶØČėNH3£»cÖŠ·Å¼īŹÆ»Ņ
B.bĶØČėNH3£¬Č»ŗóaĶØČėCO2£»cÖŠ·Å¼īŹÆ»Ņ
C.aĶØČėNH3£¬Č»ŗóbĶØČėCO2£»cÖŠ·ÅÕŗĻ”ĮņĖįµÄĶŃ֬Ǝ
D.bĶØČėCO2£¬Č»ŗóaĶØČėNH3£»cÖŠ·ÅÕŗĻ”ĮņĖį|µÄĶŃ֬Ǝ
£Ø5£©²½Öč¢ōµÄĀĖŅŗÖŠÖ÷ŅŖ³É·ÖXŹĒ²½Öč¢ņŗĶ²½Öč¢ó¶¼ÓŠµÄ²śĪļ£¬æÉŅŌ»ŲŹÕ×÷ĪŖ·ŹĮĻŹ¹ÓĆ£¬øĆ·ŹĮĻ_______(Ģī”°æÉŅŌ”±»ņ”°²»æÉŅŌ”±)Óė²ŻÄ¾»Ņ(ÓŠŠ§³É·ÖK2CO3)¹²ÓĆ£¬¼ņŹöŌŅņ£ŗ__________”£
£Ø6£©ŅŃÖŖCuClĪŖÄŃČÜÓŚĖ®µÄ°×É«³Įµķ£¬Š“³ö²½Öč¢õ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ_____________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĄūÓĆ·“Ó¦6NO2+8NH3=7N2+12H2O¹¹³Éµē³ŲµÄ·½·Ø£¬¼ČÄÜŹµĻÖÓŠŠ§Ļū³żµŖŃõ»ÆĪļµÄÅÅ·Å£¬¼õĒį»·¾³ĪŪČ¾£¬ÓÖÄܳä·ÖĄūÓĆ»ÆѧÄÜ£¬×°ÖĆČēĶ¼ĖłŹ¾£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£© 
A.µē¼«BĪŖøŗ¼«
B.µē¼«AµÄ·“Ó¦Ź½ĪŖ2NH3©6e©+6OH©=N2+6H2O
C.ČÜŅŗÖŠOH©ĶعżŅõĄė×Ó½»»»Ä¤“Ó×óĻņÓŅĒØŅĘ
D.µ±ÓŠ4.48LNO2£Ø±ź×¼×“æöĻĀ£©±»“¦ĄķŹ±£¬×ŖŅʵĵē×ÓĪŖ0.4mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŹŅĪĀĻĀ£¬½«0.10molL©1µÄŃĪĖįµĪČė20mL0.10molL©1µÄ°±Ė®ÖŠ£¬ČÜŅŗµÄpHŗĶpOHĖę¼ÓČėŃĪĖįĢå»ż±ä»ÆµÄĒśĻßČēĶ¼ĖłŹ¾£®ŅŃÖŖ£ŗpOH=©lg c£ØOH©£©£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£© 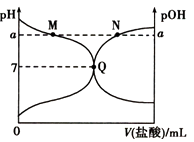
A.MµćĖłŹ¾µÄČÜŅŗÖŠc£ØNH4+£©+c£ØNH3H2O£©=c£ØCl©£©
B.QµćĖłŹ¾µÄČÜŅŗÖŠc£ØNH4+£©£¾c£ØCl©£©£¾c£ØH+£©=c£ØOH©£©
C.NµćĖłŹ¾µÄČÜŅŗÖŠc£ØNH4+£©=c£ØCl©£©
D.MµćŗĶNµćĖłŹ¾µÄČÜŅŗÖŠĖ®µÄµēĄė³Ģ¶ČĻąĶ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”潫4.6 gÄĘĶ¶Čėµ½95.4gĖ®ÖŠ£¬ĖłµĆČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹż(””””)
A.µČÓŚ4.6%B.µČÓŚ8%
C.“óÓŚ8%D.Š”ÓŚ8%
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŌŚÕęŗĖĻø°ūÖŠ£¬DNA“ęŌŚÓŚ£Ø £©
A. Ļø°ūŗĖÖŠ B. Ļø°ūÖŹÖŠ
C. Ļø°ūŗĖŗĶĻø°ūÖŹÖŠ D. Ļø°ūŗĖ”¢ĻßĮ£Ģ唢Ņ¶ĀĢĢåÖŠ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijĶ¬Ń§ĄūÓĆÉś»īÖŠ»ņŹµŃéŹŅÖŠ³£ÓƵÄĪļĘ·£¬øł¾ŻŃõ»Æ»¹Ō·“Ó¦ÖŖŹ¶ŗĶµē»ÆѧÖŖŹ¶£¬×Ō¼ŗ¶ÆŹÖÉč¼ĘĮĖŅ»øöŌµē³Ų”£ĒėĢīŠ“ĻĀĮŠæÕ°×£ŗ
(1)ŹµŃéŌĄķ£ŗFe£«2H£«===Fe2£«£«H2”ü
(2)ŹµŃéÓĆĘ·£ŗµē¼«(________”¢________)”¢Ļ”ĮņĖį”¢________”¢________”¢¶ś»ś(»ņÕßµēĮ÷±ķ)(ĢīŠ“ĖłČ±µÄŹµŃéÓĆĘ·)”£
(3)ŹµŃé×°ÖĆČēĶ¼”£

(4)Ōµē³ŲÉč¼Ę¼°×¢ŅāµÄĪŹĢā£ŗ
¢Ł°“ČēĶ¼ĖłŹ¾×°ÖĆĮ¬½ÓŗĆŹµŃéŅĒĘ÷£¬×¢Ņā¹Ū²ģ(¶ś¶äĢż)¶ś»śŹĒ·ńÓŠÉłŅō·¢³ö£¬Čē¹ūƻӊ£¬æɽ«Ōµē³ŲµÄĮ½øöµē¼«ÖŠµÄŅ»¼«½Ó“„¶ś»ś²åĶ·ÉĻµÄŅ»¼«(×¢Ņā£ŗ½Ó“„µÄĶ¬Ź±¶ś»śµÄĮķŅ»øö¼«ŹĒĮ¬½ÓŌŚŌµē³ŲµÄĮķŅ»øöµē¼«ÉĻµÄ)£¬ÕāŹ±æÉŅŌĢż¼ū¶ś»ś·¢Éś”°ąźąźąź”””±µÄÉłŅō”£ĘäŌŅņŹĒŌŚŌµē³ŲÖŠ£¬ÓÉ»ÆѧÄÜ×Ŗ»ÆĪŖ________£¬ŌŚ¶ś»śÖŠÓÖÓÉ________×Ŗ»ÆĪŖÉłŅōÕāÖÖÄÜĮ棻
¢ŚČē¹ū½«×°ÖĆÖŠµÄ¶ś»śøÄĪŖµēĮ÷±ķ£¬ŌņĢś¶¤Ó¦øĆ½ÓµēĮ÷±ķµÄ______¼«£¬µē¼«·“Ó¦Ź½ĪŖ____£¬·¢ÉśĮĖ______·“Ó¦£»
¢ŪĶ¶¤Ó¦øĆ½ÓµēĮ÷±ķµÄ__________¼«£¬µē¼«·“Ó¦Ź½ĪŖ____________________________£¬·¢ÉśĮĖ________·“Ó¦”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ±ä»ÆŹōÓŚ»Æѧ±ä»Æ£¬ĒŅ²śĪļÖŠ¼ęÓŠĘųĢ唢ŅŗĢ唢¹ĢĢåµÄŹĒ
A. ŹÆÓĶµÄ·ÖĮóB. ŹÆÓĶµÄĮŃ½ā
C. ĆŗµÄøÉĮóD. ĆŗµÄĘų»Æ
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com