
| A. | NH4Cl NaCl NaHCO3 Na2CO3 | |
| B. | NaHCO3 Na2CO3 NH4Cl NaCl | |
| C. | Na2CO3 NaHCO3 NaCl NH4Cl | |
| D. | Na2CO3 NH4Cl NaHCO3 NaCl |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:多选题
| A. | 水果、蔬菜含有丰富的维生素,若要减肥,每天只吃水果、蔬菜即可 | |
| B. | 米饭含有大量的淀粉,成人每天食用量不能超过500g | |
| C. | 要促进身体健康,饮食必须合理搭配 | |
| D. | 鸡蛋含有丰富的蛋白质,人体所需的蛋白质可由鸡蛋提供,青少年可适当多吃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳原子与碳原子之间形成的σ键比π键重叠程度大,形成的共价键强 | |
| B. | 两个原子之间形成共价键时,最多有一个σ键 | |
| C. | 乙炔分子中,共含有4个σ键,1个π键 | |
| D. | 共价单键都属于σ键,π键只存在于双键或叁键中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.3g Mg | B. | 2.7g Al | C. | 2.4 g Mg | D. | 2.8g Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯与氧气在银催化作用下生成环氧乙烷( 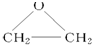 ) ) | |
| B. | 乙烷与氯气制备氯乙烷 | |
| C. | 苯和乙醇为原料,在一定条件下生产乙苯 | |
| D. | 乙醇与浓硫酸共热制备乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 L 0.1 mol•L-1的氨水中含有的NH3•H2O分子数为0.1 NA | |
| B. | 电解精炼铜时,若阳极质量减少6.4 g,则电路中转移电子数为0.2 NA | |
| C. | 标准状况下,2.24 L的二氯甲烷中含有的碳氯共价键的数目为0.2 NA | |
| D. | 一定条件下,4.6 g NO2和N2O4混合气体中含有的N原子数目为0.1 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 64n | B. | $\frac{1}{64}$n | C. | 32n | D. | $\frac{3}{64}$n |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgNO3溶液、KOH溶液、K2SO3溶液、KI溶液 | |
| B. | 苯酚溶液、CCl4溶液、氯水、氨水 | |
| C. | 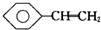 、CH3-C≡CH、福尔马林、乙醛 、CH3-C≡CH、福尔马林、乙醛 | |
| D. | NaOH溶液、FeCl2溶液、亚硫酸溶液、KCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 步骤 | 实验过程 | 实验用品 |
| Ⅰ | 将干海带灼烧灰化 | 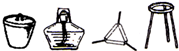 |
| Ⅱ | 将海带灰溶解、过滤 |  和①玻璃棒(玻璃仪器名称) |
| Ⅲ | 氧化滤液中的I-,反应的离子方程式为②2I-+H2O2+2H+=I2+2H2O | 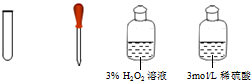 |
| Ⅳ | 取少量Ⅲ中反应后溶液于试管中,加入少量CCl4并振荡后静置,观察到③下层溶液变为紫红色,说明海带中含有碘元素. | 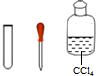 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com