
短周期主族元素A,B,C,D,E,F的原子序数依次增大,它们的原子核外电子层数之和为13。B的化合物种类繁多,数目庞大;C,D是空气中含量最多的两种元素,D,E两种元素的单质反应可以生成两种不同的离子化合物;F为同周期半径最小的元素。试回答以下问题:
(一)(1)D在周期表中的位置是 ,写出实验室制备单质F的离子方程式 。
(2)化学组成为BDF2的电子式为: ,A、C、F三种元素形成的化合物CA4F为 化合物(填 “离子”或“共价”)。
(3)化合物甲、乙由A,B,D,E中的三种或四种组成,且甲、乙的水溶液均呈碱性。则甲、乙反应的离子方程式为: 。
(4)由C,D,E,F形成的简单离子的离子半径由大到小的顺序是 (用元素离子符号表示)。
(5)元素B和F的非金属性强弱,B的非金属性 于F(填“强”或“弱”),并用化学方程式证明上述结论 。
(二)以CA3代替氢气研发氨燃料电池是当前科研的一个热点。
(1)CA3燃料电池使用的电解质溶液是2mol•L﹣1的KOH溶液,电池反应为:4 CA3+3O2=2C2+6H2O.该电池负极的电极反应式为 ;每消耗3.4g CA3转移的电子数目为 。
(2)用CA3燃料电池电解CuSO4溶液,如图所示,A、B均为铂电极,通电一段时间后,在A电极上有红色固体析出,则B电极上发生的电极反应式为 ;此时向所得溶液中加入8gCuO固体后恰好可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为 L。
(3)常温下,将除去表面氧化膜的Al、Cu片插入浓HNO3中组成原电池(图1),测得原电池的电流强度(I)随时间(t)的变化如图2所示,反应过程中有红棕色气体产生。
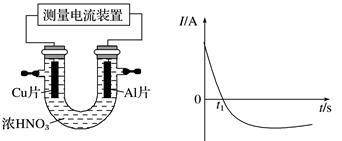
图1 图2
0~t1时,原电池的负极是Al片,此时,正极的电极反应式是 ,溶液中的H+向 极移动(填“正”或“负”),t1时,原电池中电子流动方向发生改变,其原因是 。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年重庆市高一上期中测试化学试卷(解析版) 题型:选择题
将20mL0.3mol/LAgNO3溶液与10mL0.4mol/LCaCl2溶液混合,所得溶液中离子浓度关系正确的是( )
A.c(Ca2+)>c(Cl-)>c(NO3-) B.c(Ca2+)>c(NO3-)>c(Cl-)
C.c(NO3-)>c(Ca2+)>c(Cl-) D.c(Cl-)>c(Ca2+)>c(NO3-)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西师范大学附属中学高三第一次模拟理化学试卷(解析版) 题型:选择题
在1.0L密闭容器中放入0.10 mol X,在一定温度下发生反应:X(g)  Y(g)+ Z(g) △H<0容器内气体总压强p随反应时间t的变化关系如图所示。 以下分析正确的是
Y(g)+ Z(g) △H<0容器内气体总压强p随反应时间t的变化关系如图所示。 以下分析正确的是
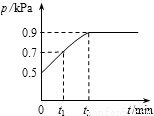
A.从反应开始到t1时的平均反应速率v(X) = 0.2/t1 mol/(L•min)
B.该温度下此反应的平衡常数K = 0.32
C.欲提高平衡体系中Y的含量,可升高体系温度或减少Z的量
D.其他条件不变,再充入0.1 mol 气体X,平衡正向移动,X的转化率增大
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期期中测试化学试卷(解析版) 题型:选择题
化学概念在逻辑上存在如右下图所示关系。对下列概念的说法正确的是
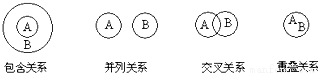
A.氧化还原反应与放热反应属于包含关系 B.溶液与胶体属于并列关系
C.化合物与碱性氧化物属于交叉关系 D.化合物与电解质属于重叠关系
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期第三次月考化学试卷(解析版) 题型:实验题
化学实验有助于理解化学知识,形成化学观念,提高探究与创新能力,提升科学素养。 某化学兴趣小组对氯及其化合物进行探究。
(1)漂白精广泛用于饮用水消毒、医院环境消毒、游泳池消毒。资料查阅:随漂白精溶液酸性的增强,溶液会变为黄绿色。出现该现象的原因为 (用离子方程式表示)。

(2)实验室可用氯气与金属铁反应制备无水三氯化铁,三氯化铁呈棕红色、易潮解,100 左右时升华。某化学兴趣小组利用下列装置(有些装置可重复使用)设计实验制备并收集无水三氯化铁。
左右时升华。某化学兴趣小组利用下列装置(有些装置可重复使用)设计实验制备并收集无水三氯化铁。

①仪器X的名称为 。
②制备三氯化铁的反应开始前,需排除装置中的空气,采取的方法是 。
③实验装置的连接顺序是a 。
(3)设计实验证明FeCL3的氧化性比I2强: 。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖南常德石门第一中学高一上期中化学试卷(解析版) 题型:选择题
下列各组中两个溶液间的反应,均可用同一离子方程式表示的是 ( )
A.CH3COOH和Na2CO3与CH3COOH和NaHCO3
B.AgNO3和HCl与Ag2SO3和HCl
C.BaCl2和Na2SO4 与Ba(OH)2与H2SO4
D.KOH和CH3COOH与Ba(OH)2与CH3COOH
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江省高三上学期12月月考化学试卷(解析版) 题型:选择题
某温度下,向2 L恒容密闭容器中充入1.0 mol A和1.0 mol B,反应:
A(g)+B(g)  C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见
C(g)经过一段时间后达到平衡。反应过程中测定的部分数据见
下表,下列说法正确的是 ( )
t/s | 0 | 5 | 15 | 25 | 35 |
n(A)/mol | 1.0 | 0.85 | 0.81 | 0.80 | 0.80 |
A.反应在前5 s的平均速率v(A)=0.17 mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(A)=0.41 mol·L-1,则反应的ΔH>0
C.相同温度下,起始时向容器中充入2.0 mol C,达到平衡时,C的转化率大于80%
D.相同温度下,起始时向容器中充入0.20 mol A、0.20 mol B和1.0 mol C,
反应达到平衡前v(正)<v(逆)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西柳州铁路第一中学高一上段考化学试卷(解析版) 题型:简答题
氧化还原反应在生产、生活中具有广泛的用途、贯穿古今。
(1)水是人体的重要组成部分,是人体中含量最多的一种物质。而“四种基本反应类型与氧化还原反应的关系”也可用右下图表达。
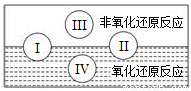
试写出有水参加的符合反应类型Ⅳ的一个化学方程式:________________,其中水为________剂。
(2)过氧化氢俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。关于双氧水,回答下列问题:
①下列反应中,H2O2既体现氧化性又体现还原性的反应是( )
A.Na2O2+2HCl═2NaCl+H2O2
B.Ag2O+H2O2 ═2Ag+O2↑+H2O
═2Ag+O2↑+H2O
C.2H2O2═2H2O +O2↑
D.3H2O2+Cr2(SO4)3 +10KOH═2K2CrO4+3K2SO4+8H2O
②保存过氧化氢的试剂瓶上最适合贴上的一个标签是( )(填序号)
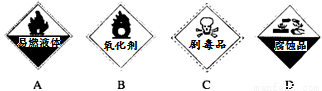
(3)焊接铜器时,可先用NH4Cl 除去其表面的氧化铜再进行焊接,该反应可表示为:
4CuO + 2NH4Cl △ 3Cu + CuCl2 + N2↑+ 4H2O
3Cu + CuCl2 + N2↑+ 4H2O
①用双线桥标明电子转移的方向和数目。
②该反应中,被氧化的元素是 ,氧化剂是 。
③还原剂与氧化产物的物质的量之比为 。
④反应中若产生0.2 mol的氮气,则有 mol的电子转移。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com