
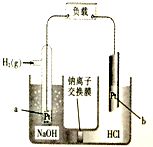
| A. | b极是负极 | |
| B. | a极电极反应式为H2-2e-═2H+ | |
| C. | 负载通过1mol电子,右池产生标况下5.6L气体 | |
| D. | 电池总反应式为:H++OH-═H2O |
分析 该反应中,a极氢气失电子发生氧化反应为负极,b极氢离子得电子放出氢气为正极,据此分析解答.
解答 解:该反应中,a极氢气失电子发生氧化反应为负极,反应式为H2-2e-+2OH-═2H2O,b极氢离子得电子放出氢气为正极,反应式为2H++2e-═H2,
A.根据以上分析,b极氢离子得电子放出氢气为正极,故A错误;
B.a极氢气失电子发生氧化反应为负极,反应式为H2-2e-+2OH-═2H2O,故B错误;
C.右池b极氢离子得电子放出氢气为正极,反应式为2H++2e-═H2,所以通过1mol电子,产生标况下11.2L气体,故C错误;
D.a极氢气失电子发生氧化反应为负极,反应式为H2-2e-+2OH-═2H2O,b极氢离子得电子放出氢气为正极,反应式为2H++2e-═H2,所以总反应式为:H++OH-═H2O,故D正确;
故选D.
点评 本题考查化学电源新型电池,侧重考查原电池原理,明确正负极的判断、电极反应式的书写即可解答,难点是电极反应式的书写.


科目:高中化学 来源: 题型:解答题
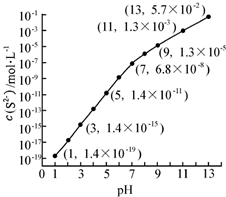 (1)25℃,在0.10mol•L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图(忽略溶液体积的变化、H2S的挥发).
(1)25℃,在0.10mol•L-1H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图(忽略溶液体积的变化、H2S的挥发).查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+、Cl-、Ca2+ | B. | Mg2+、SO42-、OH- | C. | Na+、SO32-、H+ | D. | H+、K+、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C60是英国和美国化学家共同发现的,体现了国际科技合作的重要性 | |
| B. | 门捷列夫在前人工作的基础上发现了元素周期律,表明科学研究既要继承又要创新 | |
| C. | 科恩和波普尔因理论化学方面的贡献获诺贝尔化学奖,意味着化学已成为以理论研究为主的学科 | |
| D. | 维勒用无机物合成了尿素,突破了无机物与有机物的界限 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用pH试纸测氯水的pH | |
| B. | 用磨口玻璃瓶保存NaOH溶液 | |
| C. | 中和滴定时锥形瓶使用前需用待测液润洗 | |
| D. | 用CS2可除去试管内壁残留的S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
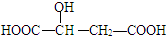 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 苹果酸中能发生酯化反应的官能团有2种 | |
| B. | 1mol苹果酸可与3mol NaOH发生中和反应 | |
| C. | 1mol苹果酸与足量金属Na反应生成生成1molH2 | |
| D. | HOOC-CH2-CH(OH)-COOH与苹果酸互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该元素的单质在常温下跟水反应不如钠剧烈 | |
| B. | 该元素的原子半径比钾的原子半径小 | |
| C. | 该元素的碳酸盐难溶于水 | |
| D. | 该元素最高价氧化物的水化物能使Al(OH)3溶解 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种类最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.回答下列问题:
原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种类最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com