
【题目】氮氧化物会形成光化学烟雾和酸雨,可采取下列方法对氰氧化物进行处理。
(1) SNCR脱硝技术的原理:
 ____________
____________
(2) NSR (NOx储存还原)工作原理:
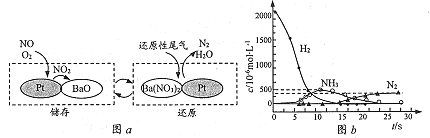
NOx的储存和还原在不同时段交替进行,如图a所示。
①NOx储存转化为Ba(NO3)2过程中,参加反应的NO和02的物质的量之比为_________________。
②H2还原Ba(NO3)2的过程分两步进行,图b表示该过程相关物质浓度随时间的变化关系。第一步反应的化学方程式为__________________。
(3)SCR消除氮氧化物的反应原理:![]()
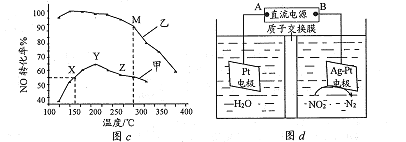
其他条件相同,某密闭容器中分别投入NH3、NO、O2,在甲、乙两种催化剂作用下,NO转化率与温度的关系如图c所示。在催化剂甲作用下,图中Y点处(对应温度为210℃)NO的转化率一定不是该温度下的平衡转化率的原因是__________________。工业实际选择催化剂乙的原因是___________________。
(4)①用石灰乳吸收氨的氧化物,原理为:
![]()
为使吸收充分![]() ___(选填“≥”或“≤”)l。
___(选填“≥”或“≤”)l。
②目前可采用电解的方法除去废水中的NO2-,原理如图d所示。写出阴极的电极反应式:__________________。
【答案】 ΔH=–2735.6kJ·mol–1 4∶3 8H2+Ba(NO3)2![]() BaO+2NH3+5H2O 平衡转化率是该温度下的最大转化率,此时Y点NO的转化率明显低于同温度下乙作催化剂时NO的转化率 在低温下,使用催化剂乙,NO转化率很高 ≥ 2NO
BaO+2NH3+5H2O 平衡转化率是该温度下的最大转化率,此时Y点NO的转化率明显低于同温度下乙作催化剂时NO的转化率 在低温下,使用催化剂乙,NO转化率很高 ≥ 2NO![]() +4H2O+6e- ===N2+8 OH— (若答2NO
+4H2O+6e- ===N2+8 OH— (若答2NO![]() +8H++6e- ===N2+4H2O也正确)
+8H++6e- ===N2+4H2O也正确)
【解析】(1)已知:
①4NO(g)+4NH3(g)+O2(g)=4N2(g)+6H2O(g) △H=-1627.2kJ/mol
②6NO(g)+4NH3(g)=5N2(g)+6H2O(g) △H=-1807.0kJ/mol
③2NO(g)+O2(g)=2NO2(g) △H=-113.0kJ/mol
则根据盖斯定律可知(①-③)×3-②即得到反应6NO2(g)+8NH3(g)=7N2(g)+12H2O(g) △H=-2735.6kJ/mol;
(2)①反应中氮元素化合价从+2价升高到+5价,失去3个电子,氧气中氧元素化合价从0价降低到-2价,得到2个电子,根据电子得失守恒可知参加反应的NO和02的物质的量之比为4∶3;②根据图像可知第一步反应的还原产物是氨气,则结合图a可知第一步反应的化学方程式为8H2+Ba(NO3)2![]() BaO+2NH3+5H2O。
BaO+2NH3+5H2O。
(3)由于平衡转化率是该温度下的最大转化率,此时Y点NO的转化率明显低于同温度下乙作催化剂时NO的转化率,所以在催化剂甲作用下,图中Y点处(对应温度为210℃)NO的转化率一定不是该温度下的平衡转化率。根据图像可知在低温下,使用催化剂乙,NO转化率很高,所以工业实际选择催化剂乙;
(4)①由于NO不能与氢氧化钙反应,而NO2可以,所以为使吸收充分,NO2与NO的体积之比应该≥l。②阴极NO2-得到电子发生还原反应生成氮气,因此阴极的电极反应式为2NO2-+4H2O+6e-=N2+8OH—。


科目:高中化学 来源: 题型:
【题目】利用下图装置可以进行实验并能达到实验目的的是
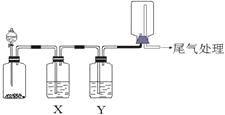
选项 | 实验目的 | X中试剂 | Y中试剂 |
A[] | 用MnO2和浓盐酸制取并收集纯净干燥的Cl2 | 饱和食盐水 | 浓硫酸 |
B | 用Cu与稀硝酸制取并收集纯净干燥的NO | 水 | 浓硫酸 |
C | 验证电石与饱和食盐水反应生成的气体的性质并收集 | CuSO4溶液 | KMnO4 |
D | CaCO3和稀盐酸制取并收集纯净干燥的CO2 | 饱和NaHCO3溶液 | 浓硫酸 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】需要配制500 mL 0.5 mol·L-1氢氧化钠溶液,经测定实际所配氢氧化钠溶液的浓度为0.45 mol·L-1。可能的原因是( )
A. 转移时溶液没有冷却至室温 B. 容量瓶没有烘干
C. 称量氢氧化钠固体时砝码放反了 D. 定容时仰视读数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃与氢气发生反应后能生成(CH3)2CHCH2CH3,则该烃不可能是
A. 2-甲基-2-丁烯 B. 3-甲基-1-丁烯
C. 2.3-二甲基-1-丁烯 D. 3-甲基-1-丁炔
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有甲、乙两种物质:

(1)乙中含有的官能团的名称为__________________(不包括苯环)。
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
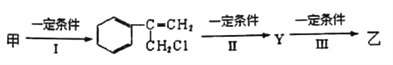
反应I的化学其中反应I的反应类型是____________________,反应II的条件是________,反应III的化学方程式为_________________(不需注明反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】掌握仪器的名称、组装及使用方法是中学化学实验的基础,根据下图所示实验装置,回答下列问题。
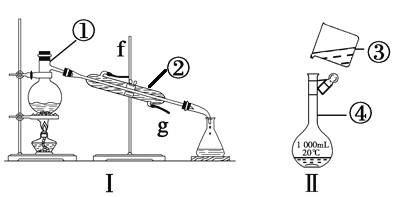
(1)写出下列仪器的名称:①________,②________,④________。
(2)仪器①~④中,使用时必须检查是否漏水的是________(填序号)。
(3)若利用装置Ⅰ分离酒精和水的混合物,还缺少的仪器________,将仪器补充完整后进行的实验操作的名称为________;②的进水口是________(填“f”或“g”)。
(4)现需配制250 mL、0.2 mol·L-1NaCl溶液,装置Ⅱ是某同学转移溶液的示意图,指出图中的错误操作:_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)100mL0.2mol/L Na2SO4溶液中含有SO42﹣___________________mol,Na+的物质的量浓度是_________________mol/L。
(2)5molCO2在标准状况下所占的体积约为________L;所含氧原子的数目约为_______个。
(3)3.01×1023个OH﹣的物质的量为___mol,质量为______g,含有电子的物质的量为_______mol,这些OH﹣与___________mol NH3的质量相同。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了除去KCl溶液中少量的MgCl2、MgSO4,从稀盐酸、Na2CO3、Ba(NO3)2、K2CO3、Ba(OH)2溶液中,选择A、B、C 3种试剂,按图中的实验步骤进行操作:
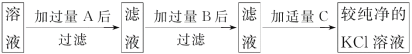
(1)3种试剂的化学式:A______,B______,C______。
(2)加过量A的原因是___________________________________________________________,有关反应的化学方程式为________________________________________________________________。
(3)加过量B的原因是______________________________________________________,有关反应的化学方程式为_____________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com