
| A. | 用Na2O2和H2O 反应制备O2:Na2O2+H2O═2Na++2OH-+O2↑ | |
| B. | 用氢氧化钠溶液除去金属铝表面的氧化膜:Al2O3+2OH-═2AlO2-+H2O | |
| C. | 用食醋除去水瓶中的水垢:2CH3COOH+CO32-═2CH3COO-+CO2↑+H2O | |
| D. | 等体积、等浓度的Ba(OH)2浓溶液和NH4HCO3 浓溶液混合后并加热Ba2++OH-+HCO3-═BaCO3↓+2H2O |
分析 A.原子个数不守恒;
B.二者反应生成偏铝酸钠和水;
C.碳酸钙为沉淀,应保留化学式;
D.二者反应生成碳酸钡、一水合氨和水.
解答 解:A.用Na2O2和H2O 反应制备O2,离子方程式:N2a2O2+2H2O═4Na++4OH-+O2↑,故A错误;
B.用氢氧化钠溶液除去金属铝表面的氧化膜,离子方程式:Al2O3+2OH-═2AlO2-+H2O,故B正确;
C.用食醋除去水瓶中的水垢,离子方程式:2CH3COOH+CaCO3═2CH3COO-+CO2↑+H2O+Ca2+,故C错误;
D.等体积、等浓度的Ba(OH)2浓溶液和NH4HCO3 浓溶液混合后并加热,离子方程式:Ba2++2OH-+HCO3-═BaCO3↓+H2O+NH3•H2O,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,明确反应实质及离子方程式书写方法是解题关键,注意化学式拆分,注意反应物用量对反应的影响,选项D为易错选项.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
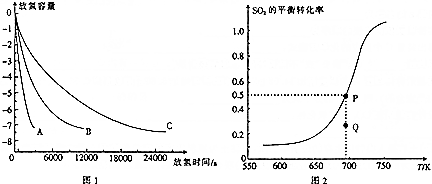
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
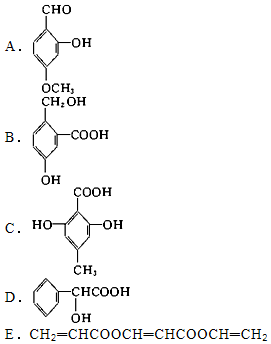
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 对不可回收垃圾常用的处理方法有卫生填埋、堆肥和焚烧 | |
| B. | 制造玻璃是复杂的物理变化,玻璃的组成不同,性能不同 | |
| C. | BaSO4在医学上用作钡餐 | |
| D. | 固体煤经处理变为气体燃料后,可以减少SO2和烟尘的污染,且燃烧效率高 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 取一定量固体,溶解,向溶液中滴加适量AgNO3溶液,观察到有白色沉淀生成,说明原固体中一定含有NaCl | |
| B. | 取一定量固体,溶解,向溶液中加入适量CaO粉末,充分反应后观察到有白色沉淀生成,说明原固体中一定含有Na2CO3 | |
| C. | 取一定量固体,溶解,向溶液中通入足量的CO2,观察到有晶体析出,说明原固体中一定含有Na2CO3 | |
| D. | 称取3.80g固体,加热至恒重,质量减少了0.620g.用足量稀盐酸溶解残留固体,充分反应后,收集到0.880g气体,说明原固体中仅含有Na2CO3和NaHCO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某元素从化合态变为游离态时,该元素一定被还原 | |
| B. | 含金属元素的离子一定是阳离子 | |
| C. | 金属单质只有还原性,金属阳离子不一定只有氧化性 | |
| D. | 不同的气体,若体积不同,则它们所含的分子数一定不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
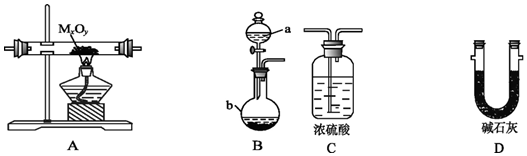
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
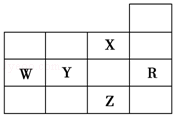 如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )| A. | W元素的电负性大于Y元素的电负性 | |
| B. | X元素是电负性最大的元素 | |
| C. | p能级未成对电子最多的是Z元素 | |
| D. | Y、Z的阴离子电子层结构都与R原子的相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com