
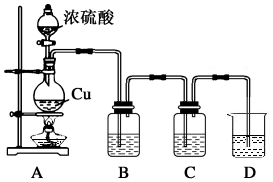
���� ��1����Ӧ����ȡ�����װ�ã����Է�Ӧ��ʼǰ����Ҫ����װ�õ������ԣ�
��2��Cu��Ũ���ᷴӦ��������ͭ�����������ˮ���ݴ�д����Ӧ�Ļ�ѧ����ʽ��
��3������������ʹƷ����Һ��ɫ��
��4��������������ˮ�е�������Ӧ�������������ᣬ������Һ�ɵ�����ɫ��Ϊ��ɫ��������������Ļ��ϼ������ǻ�ԭ����
��5���ձ�D��β��������װ�ã�ʢװ���Լ���Ũ�Ƚϴ�Ŀ����Ե�ǿ����Һ�������������ն����������壻
��6���ɷ�ӦCu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O������Ӧ����2mol����ת�ƣ�������1mol��SO2��
��� �⣺��1����Ӧ����ȡ�����װ�ã����Է�Ӧ��ʼǰ����Ҫ����װ�õ������ԣ��ʴ�Ϊ������װ�õ������ԣ�
��2��Cu��Ũ���ᷴӦ��������ͭ�����������ˮ����Ӧ�Ļ�ѧ����ʽΪCu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
�ʴ�Ϊ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
��3������������ʹƷ����Һ��ɫ������ȷ����SO2���ɵ�������Ʒ����Һ��ɫ���ʴ�Ϊ��Ʒ����Һ��ɫ��
��4��������������ˮ�е�������Ӧ�������������ᣬ������Һ�ɵ�����ɫ��Ϊ��ɫ��������������Ļ��ϼ������ǻ�ԭ�������л�ԭ�ԣ��ʴ�Ϊ����ɫ����ԭ��
��5���ձ�D��β��������װ�ã�ʢװ���Լ���Ũ�Ƚϴ�Ŀ����Ե�ǿ����Һ����������������Һ�������������ն����������壬�ʴ�Ϊ��NaOH����ֹSO2й©��Ⱦ������
��6���ɷ�ӦCu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O������Ӧ����2mol����ת�ƣ�������1mol��SO2����״���µ����Ϊ22.4L���ʴ�Ϊ��22.4 L��
���� ���⿼����Ũ������ͭ�ķ�Ӧ������Ũ��������ʡ���������������ǽ����Ĺؼ�����Ŀ�ѶȲ���


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��Al3+ǡ����ȫ����ʱ������Ba��OH��22 mol | |
| B�� | ��SO42-ǡ����ȫ����ʱ��Al3+ȫ��ת��ΪAl��OH��3 | |
| C�� | ������Һ�м���1.5mol Ba��OH��2ʱ����Ӧ�����������ӷ���ʽ��ʾ��2Al3++3 SO42-+3Ba2++6OH-�T2Al��OH��3��+3BaSO4�� | |
| D�� | ���ż����Ba��OH��2�����ʵ������������������ʵ����������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��֯���Ũ������ | B�� | Ƥ����մ��Ũ������� | ||
| C�� | ����������ζ | D�� | ����������ˮ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ѹǿp p��=p����2p�� | |
| B�� | SO3������m m��=m����2m�� | |
| C�� | c��SO2����c��O2��֮��k k��=k����2k�� | |
| D�� | ��Ӧ�ų���������������ֵQ Q��=197-Q����2Q�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeCl3��Һ��FeCl2����ͨ������Cl2 | |
| B�� | Fe2O3���壨Al2O3���������ռ���Һ������ | |
| C�� | Cl2���壨HCl����ͨ��NaOH��Һϴ������� | |
| D�� | Na2CO3���壨NaHCO3�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
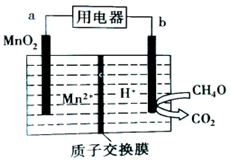
| A�� | a��Ϊ������������ԭ��Ӧ | |
| B�� | b���ĵ缫��ӦΪCH4O-6e-+H2O=CO2+6H+ | |
| C�� | ���Ӵ�b���������õ�������a�� | |
| D�� | �ŵ�ʱH+�����ӽ���Ĥ��������Ҳ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������Һ�м�������İ�ˮ��Al3++3NH3•H2O�TAl��OH��3��+3NH4+ | |
| B�� | �Ȼ�þ��Һ�м�������������Һ��Mg2++2OH-�TMg��OH��2�� | |
| C�� | ��Ƭ�������ŨNaOH��Һ��2Al+2OH-+2H2O�T2AlO2-+3H2�� | |
| D�� | ��ͭƬ�������ϡHNO3��Һ�У�3Cu+8HNO3�T3Cu2++6NO3-+2NO��+4H2O |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com