
【题目】物质在水中可能存在电离平衡、水解平衡和沉淀溶解平衡。根据所学知识回答下列问题:
(1)下列方法中,可以使0.10mol/LCH3COOH溶液中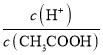 值增大的措施是_______________(填序号)。
值增大的措施是_______________(填序号)。
a.加水稀释b.加入少量CH3COONa固体 c.加入少量冰醋酸d.通入少量HCl气体 e.加少量烧碱溶液 f.升高温度
(2)t℃时,水的离子积常数Kw=1×10-12。
①该温度下,若100体积pH=a的H2SO4溶液与1体积pH=b的NaOH溶液混合后溶液呈中性,则a+b=_________。
②该温度下,pH=2的某酸HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5。试分析其原因:_______________________;该混合溶液中:c(A-)-c(Na+)=______________________mol/L(填数值)。
(3)25℃下,有浓度均为0.1mol/L的三种溶液:a.NaHCO3;b.NaClO;c.CH3COONa。(已知25℃时电离常数:H2CO3 K1=4.4×10-7,K2=4.7×10-11;HClO K=3.0×10-8;CH3COOH K=1.8×10-5)
①三种溶液pH由小到大的顺序为:_______________________________(填序号)。
②溶液a的pH大于8,则溶液中c(H2CO3)_____c(CO32-)(填“>”、“<”或“=”)。
(4)已知25℃时,Ksp(AgCl)=1.8×10-10,现将足量氯化银分别放入:
a.100mL蒸馏水中;
b.100mL0.2mol/LAgNO3溶液中;
c.100mL0.1mol/L氯化铝溶液中;
d.100mL0.1mol/L盐酸溶液中。
充分搅抖后,相同温度下银离子浓度由大到小的顺序是________________(填写序号);b中氯离子的浓度为_________________。
【答案】a、d、f 14 HA为弱酸,HA中和NaOH后,混合溶液中还剩余较多的HA,可继续电离出H+,使溶液的pH=5 9.9×10-6或10-5-10-7 c<a<b > b>a>d>c 9×10-10mol/L
【解析】
(1)a.加水稀释醋酸,c(H+)、c(CH3COOH)均减小,但由于促进了醋酸的电离,c(CH3COOH)减少量大于c(H+),所以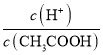 值增大,a项正确;
值增大,a项正确;
b.加CH3COONa固体,由于CH3COO-对CH3COOH的电离起着抑制作用,则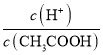 值减小,b项错误;
值减小,b项错误;
c. 加入少量冰醋酸,醋酸浓度增大,弱电解质的浓度越大,电离程度越小,则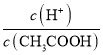 值减小,c项错误;
值减小,c项错误;
d. 通入少量HCl气体,溶液中的c(H+)明显增大,平衡左移,c(CH3COOH)略微增大,则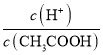 值增大,d项正确;
值增大,d项正确;
e. 加少量烧碱溶液,溶液中的c(H+)明显减小,平衡右移,c(CH3COOH)略微减小,则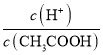 值减小,e项错误;
值减小,e项错误;
f. 升高温度,平衡右移,则c(H+)增大,c(CH3COOH)减小,所以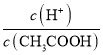 值增大,f项正确;
值增大,f项正确;
故选adf;
(2)①若100体积pH=a的H2SO4溶液中氢离子的物质的量浓度为10-amol/L,1体积pH=b的NaOH溶液中氢氧根离子的物质的量浓度为10b-12mol/L,混合溶液呈中性,则n(H+)=n(OH-),即100×10-amol/L=1×10b-12mol/L,所以a+b=14;
②pH=2的某酸HA溶液和pH=10的NaOH溶液等体积混合后,若恰好完全反应,如果酸是强酸,则盐溶液呈中性,实际上溶液呈酸性,则HA为弱酸,HA与NaOH反应后,混合溶液中还剩余较多的HA分子,可继续电离出H+,使溶液pH=5;该溶液中存在电荷守恒为c(A-)+c(OH-)=c(Na+)+c(H+),则c(A-)-c(Na+)= c(H+)-c(OH-)=(10-5-10-7)mol/L=9.9×10-6mol/L;
(3)已知酸性的强弱顺序为:CH3COOH>H2CO3>HClO;
①弱酸的酸性越弱,则对应的酸根离子水解程度越大,浓度相等时溶液的碱性越强,三种溶液pH由小到大的顺序为c<a<b;
②NaHCO3溶液的pH大于8 显碱性,HCO3-的水解程度大于其电离程度,则溶液中c(H2CO3)>c(CO32-);
(4)a.100mL蒸馏水中,c(Ag+)=![]() =1.34×10-5mol/L;
=1.34×10-5mol/L;
b. 100mL0.2mol/LAgNO3溶液中c(Ag+)为0.2mol/L,抑制沉淀溶解平衡;
c. 100mL0.1mol/L氯化铝溶液中c(Cl-)为0.3mol/L,则c(Ag+)=6×10-10mol/L;
d. 100mL0.1mol/L盐酸溶液中c(Cl-)为0.1mol/L,则c(Ag+)=1.8×10-9mol/L;
综上银离子浓度大小顺序为b>a>d>c;
b中100mL0.2mol/LAgNO3溶液中c(Ag+)为0.2mol/L,故c(Cl-)=![]() mol/L=9×10-10mol/L。
mol/L=9×10-10mol/L。


 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
【题目】某烷烃相对分子质量为86,如果分子中含有3个—CH3、2个—CH2—和1个![]() ,则该结构的烃的一氯取代物最多可能有的种类(不考虑立体异构)
,则该结构的烃的一氯取代物最多可能有的种类(不考虑立体异构)
A. 9B. 6C. 5D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值。下列说法正确的是( )
A. 5NH4NO3![]() 2HNO3+4N2↑+9H2O反应中,生成28gN2,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28gN2,转移的电子数目为3.75NA
B. 室温下,0.2mol·L-1的Na2SO4溶液中含Na+数目为0.4NA
C. 标准状况下,NA个HF分子所占的体积约为22.4L
D. 高温下,0.2molFe与足量水蒸气反应,生成的H2分子数目为0.3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中依据热化学方程式得到的对应结论正确的是
热化学方程式 | 结论 | |
A | 稀溶液中:H+(aq)+OH-(aq)=H2O (l) △H=-57.3kJ.mol-1 | 将稀硫酸与氢氧化钡溶液混合后,若有1molH2O 生成,则放出的能量为57.3kJ |
B | Sn(s,灰) | 锡制品在炎热的夏天更容易损坏 |
C | P4(s,白磷)=4P(s,红磷) △H=-29.2kJ.mol-1 | 常温下红磷比白磷更稳定 |
D | C3H8(g)+5O2(g)=3CO2 (g)+4H2O(g) △H=-2043.9kJ.mol-1 | C3H8的燃烧热△H=-2043.9kJ.mol-1 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解Na2SO4溶液联合生产硫酸和烧碱溶液的装置如下图所示,其中阴极和阳极均为惰性电极。测得同温同压下,气体甲与气体乙的体积比约为1:2。下列说法正确的是( )
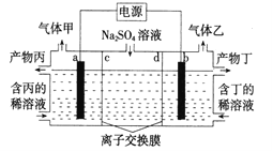
A.b 极与电源的正极相连
B.产物丙为NaOH 溶液
C.离子交换膜d 为阴离了交换膜(允许阴离子通过)
D.a 电极反应式为2H2O-4e-=4H++O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分下图中X是无支链的、具有果香味的合成香料,可用于调配多种果香型香精。已知
D在标准状况下的密度为1.25 g/L,其产量可以用来衡量一个国家石油化工发展水平。E是生活
中常见的一种有机物。各物质间转化关系如下:
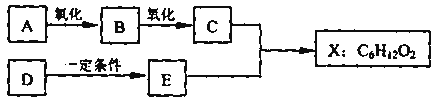
请回答下列问题。
(1)A的名称是________________________。
(2)B中所含的官能团是________________。
(3)C+E![]() X的化学反应类型是___________________反应。
X的化学反应类型是___________________反应。
(4)写出任意两种与A具有相同官能团的A的同分异构体的结构简式 (不含A):_________。
(5)X与氢氧化钠溶液反应的化学方程式是______________________________。
(6)以D为原料生产一种常见塑料的化学方程式是___________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
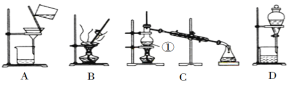
(1)在装置A和装置B中都用到玻璃棒,装置A中玻璃棒的作用是__,装置B中玻璃棒的作用是__,防止蒸发皿内溶液因局部过热而溅出。
(2)装置C中①的名称是__,①中加入沸石的作用是__,冷却水的方向是__。
(3)从氯化钠溶液中得到氯化钠固体,选择装置__(填代表装置图的字母,下同);除去自来水中的Cl等杂质,选择装置__。检验自来水中Cl-是否除净的方法:取少量锥形瓶中的水于洁净试管中,滴加__,不产生白色沉淀表明Cl已除净。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有稀硫酸和稀硝酸的混合溶液,已知其中稀硫酸和稀硝酸的浓度均为2 mol·L-1。取10mL混合酸,向其中加入1.92g铜粉,反应结束后,在标准状况下可收集到气体体积为(假设HNO3只被还原为NO)
A.0.224LB.0.336LC.0.448LD.0.672L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com