
| A、①④⑤⑥ | B、①②③④⑤ | C、①④ | D、①②③ |


科目:高中化学 来源: 题型:
| A、“雾霾”与“风雨雷电”一样属于一种自然现象 | B、塑化剂是一种应用很广的化工塑料软化剂,可大量添加到婴幼儿玩具中 | C、利用潮汐能发电能达到节能减排的目的 | D、PM2.5的产生与人类活动无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、利用风能发电、太阳能热水器、无磷洗衣粉等均有利于降低大气中的二氧化碳 | B、蛋白质、淀粉、纤维素都能在人体内水解并提供能量 | C、使用聚乙烯(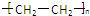 )塑料制品比使用聚乳酸 ( )塑料制品比使用聚乳酸 (  )塑料制品更环保 )塑料制品更环保 | D、酶催化反应具有高效、专一、条件温和等特点,化学模拟生物酶对环境保护、节能减排具有重要意义 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH2═CH2 | B、CH3CH═CH2 | C、CH3CH3 | D、CH2═CHCH═CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
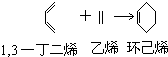
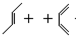 →
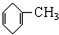
→
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、小苏打可与酸反应,可用作治疗胃酸过多的药剂 | B、氯化铝是电解质,可电解其水溶液获得金属铝 | C、SO2具有漂白性,可用于将银耳漂白为“雪耳” | D、二氧化硅具有导电性,可用于生产光导纤维 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com