
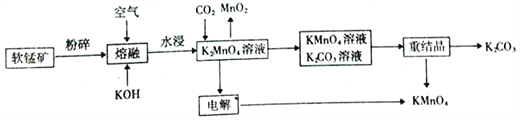
����Ŀ��������ؿ�������������������ѧ��ѧ����������������ҵ��,�����̿�( ��Ҫ�ɷ�MnO2)�Ƹ�����ص���������(���������Ͳ���ʡ��):
��ش��������⣺
��1���ڡ�ˮ���������У����K2MnO4������(������K2MnO4�����롰�ۿ顱����֮��)�Ĵ�ʩ��_______( ����д������)��
��2�������ڡ������з�����Ӧ�Ļ�ѧ����ʽΪ___________��
��3��CO2 ��K2MnO4��Ӧ�����ӷ���ʽΪ___________��
��4������⡱������ʹ�õ��Ƕ��Ե缫����:
��������Ӧ�ķ���ʽΪ__________��
������������Һ��pH��__________��(�������С�� �� ���䡱)��
��5�������������в�����Mn2+��Ի��������Ⱦ����ҵ�ϣ�ͨ������pHʹ��ˮ�е�Mn2+�γ�Mn(OH)2 ��������pH=10ʱ����Һ�е�c(Mn2+)=______(��֪:Ksp[Mn(OH)2]=2.0��10-13��������ݾ��ڳ����²ⶨ)��
���𰸡� �����ۿ顱���顢���ȡ�����ȣ� 2MnO2+O2+4KOH![]() 2K2MnO4+2H2O 3MnO42-+2CO2=2MnO4-+MnO2��+2CO32- MnO42--e-=MnO4- ���� 2.0��10-5mol/L
2K2MnO4+2H2O 3MnO42-+2CO2=2MnO4-+MnO2��+2CO32- MnO42--e-=MnO4- ���� 2.0��10-5mol/L
����������1���ڡ�ˮ���������У����K2MnO4�����ʣ�ʵ�ʾ����Ƴ���ѧϰ����μ����ܽ⣬���Դ��ǽ��裬���ȣ�����ȷ�����
��2�����������������ش������ÿ����е�������MnO2����Ϊ����أ���������һ����ˮ�����ݻ��ϼ�������Ⱥ�ԭ�Ӹ����غ���ƽ�����õ���2MnO2+O2+4KOH![]() 2K2MnO4 + 2H2O��
2K2MnO4 + 2H2O��
��3����ͼ�п������������Һ��ͨ�������̼���壬�õ�������ء��������̺�̼��أ����ݻ��ϼ�������Ⱥ�ԭ�Ӹ����غ���ƽ�����õ���3MnO42-+2CO2=2MnO4-+ MnO2�� + 2CO32-��
��4���ٵ���������Һ��Ŀ���ǵõ�������أ����������ķ�Ӧһ�������������ʧ���ӵõ�����������ӣ���ӦΪ��MnO42--e-=MnO4-��
�ڵ�������Ӧ����ˮ����������ӵõ���ת��Ϊ����������ˮ��������������ӻ�ʣ������Һ�У���Ũ����������������������Һ��pH������
��5����pH=10ʱ����Һ�е�c(H+)=1��10-10mol/L��c(OH-)=1��10-4mol/L�����Ե�pH=10ʱ����Һ�е�c(Mn2+)=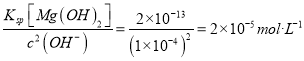 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)�ڷ�ӦA(g)+3B(g)��2C(g)�У���������A��ʾ�ĸ÷�Ӧ�Ļ�ѧ��Ӧ����Ϊ0.2 mol��L1��min1����������B��ʾ�˷�Ӧ�Ļ�ѧ��Ӧ����Ϊ________mol��L1��min1��
(2)��2 L���ܱ������У�����2 mol N2��3 mol H2����һ�������·�����Ӧ��3 s����N2Ϊ1.9 mol������H2��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ____________________________��
(3)��10 mol A��5 mol B�����ݻ�Ϊ10 L���ܱ������У�ij�¶��·�����Ӧ��3A(g)+B(g) ![]() 2C(g)�������2 s�ڣ�����A��ƽ������Ϊ0.06 mol��L1��s1������2 sʱ����������______ mol A����ʱC�����ʵ���Ũ��Ϊ________��
2C(g)�������2 s�ڣ�����A��ƽ������Ϊ0.06 mol��L1��s1������2 sʱ����������______ mol A����ʱC�����ʵ���Ũ��Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��������һ��������ƿ�������������й©�����д�����ƿ�ķ����Ϻ�������
A.�Ѹ�ƿ��������У���ʯ������B.�Ѹ�ƿ�Ƶ�С����
C.�Ѹ�ƿ̧���·�ڵĵط�������D.�Ѹ�ƿ̧���Ϸ�ڵĵط�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ΪHCl��NaCl��NaOH��Cl2������Һ�����������ǵ�һ���Լ�
A.AgNO3��ҺB.��̪��ҺC.��ɫʯ����ҺD.����ʳ��ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ǧ���ơ����Ҵ��¡����۰����������ǽ���������Ŀ�ĵ���������������ý�屨���ӱ��ȷ������ȵش��ڳ����ģ�Ĺ�ҵ��ˮ���ӣ����۰�������ˮ��������������Ŀǰ�����ö��ַ�������ˮ���д���������ˮ��Դ״����
��1�����������õ�������,��ˮ�е�NH4+����������Ӧ������NO3-��������Ӧ�������仯ʾ��ͼ����:
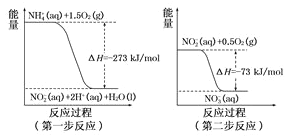
�ٵ�һ����Ӧ��______��Ӧ(ѡ����ȡ������ȡ�)������������_________��1mol NH4+ (aq)ȫ��������NO3- (aq)���Ȼ�ѧ����ʽΪ_____________��
��һ��������,���ˮ�м���CH3OH,��HNO3��ԭ��N2�����ù�����CH3OH��Ӧ����CO2,��μӷ�Ӧ�Ļ�ԭ���������������ʵ���֮��Ϊ______.
��2����������(ClO2)��һ�ֻ���ɫ���Ȼ�ɫ�����壬�ǹ����Ϲ���Ϊ��ȫ��������ɫ������,����Ͷ���ˮ�������Ⱦ�
�ٶ������ȿ��Խ���ˮ�е��軯��(CN-)��������������Ⱦ����.д�����ӷ���ʽ________��
�ڷ�ˮ�е��ؽ������ӵ�Σ���Ժܴ��������ܹ�����������Һ�аѶ��������������ɲ�����ˮ�Ķ�������(MnO2)��д����Ӧ�����ӷ���ʽ_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��0.2L1mol��L-1��KCl��Һ��0.5L1mol��L-1��FeCl3��Һ�У�Cl-��Ũ��֮����
A.1��3B.3��1C.1��1D.2��15
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�������ֵ������������ȷ���ǣ� ��
A.0.1molCl2�����������ϡNaOH��Һ��Ӧת�Ƶ�������Ϊ0.1NA
B.25��ʱ��pH=13��1.0L Ba��OH��2��Һ�к��е�OH����ĿΪ0.2NA
C.��״���£�22.4LCHCl3���еķ�����ΪNA
D.1L 0.1molL��1��������Һ����������ĿΪ0.1NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ��ش��������⣺
��1����״���£�1.12LCH4������Ϊ_______g��
��2����3.2gSO2������Oԭ������ȵ�NO2������Ϊ_______g��
��3������500mL1.0mol��L-1CuSO4��Һʱ������Һϴ�Ӻ�ҡ������ƿ������Һ�彦������������Һ���ʵ���Ũ���_______(ѡ����ƫ��������ƫ����������Ӱ����)��
��4����2.0mol��L-1Na2SO4��Һ��1.0mol��L-1H2SO4��Һ��������(�����Ϻ���Һ�����Ϊ�������֮��)����SO42-�����ʵ���Ũ��Ϊ_______mol��L-1��
��5��Ũ��ˮ�����ڼ��������ܵ��Ƿ�©������ԭ����8NH3+3Cl2=6NH4Cl+N2���÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ_______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�������ԭ��Ӧ��˵��������ǣ� ��
A. �������õ��ӣ���ԭ��ʧ����
B. ijԪ�شӻ���̬������̬�����ܱ�����Ҳ���ܱ���ԭ
C. ��ʧȥ���ӵ�ԭ�ӣ���һ���õ���
D. һ��Ԫ�ر�������һ������һ��Ԫ�ر���ԭ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com