
下列说法中错误的是
A. 历史上很多种元素是通过原子光谱发现的
B. 鉴别晶体与非晶体,最为科学的方法是X射线衍射法
C. 前36号元素中基态电子排布未成对电子数最多的元素, 在第四周期第IIIB族
D. 金属性越强的金属元素,第一电离能不一定就越小
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案科目:高中化学 来源:2016-2017学年湖南省益阳市高二下学期3月月考化学试卷(解析版) 题型:实验题
探究苯与溴的取代反应,甲用如图装置Ⅰ进行如下实验:
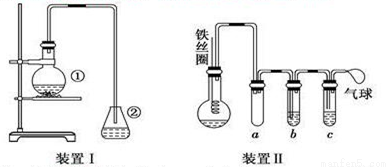
将一定量的苯和液溴放在烧瓶中,同时加入少量铁屑,3~5 min后发现装有AgNO3溶液的锥形瓶中有浅黄色的沉淀生成,即证明苯与溴发生了取代反应。
(1)装置I中①的化学方程式为: ___________________________________,
(2)①中长导管的作用是______________________________________________。
(3)烧瓶中生成的褐色油状液滴的成分是__________________________,要想得到纯净的产物,可用____________试剂洗涤。。
(4)甲做实验时,乙观察到烧瓶中液体沸腾并有红棕色气体从导管中逸出,提出必须先除去红棕色气体,才能验证锥形瓶中的产物,原因是___________。
(5)乙同学设计如图所示装置Ⅱ,并用下列某些试剂完成该实验。可选用的试剂是:苯;液溴;浓硫酸;氢氧化钠溶液;硝酸银溶液;四氯化碳。
a的作用是_____________________; b中的试剂是___________________;
比较两套装置,装置Ⅱ的主要优点是:(答出一点即可)_________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省漯河市高二3月月考化学试卷(解析版) 题型:选择题
通式为CnH2n-2的某烃与足量氧气在密闭容器中完全燃烧,150℃时,若反应前后压强不变,则此烃分子式中的n值为
A. 2 B. 3 C. 4 D. 5
查看答案和解析>>
科目:高中化学 来源:2017届四川省广元市高三第二次高考适应性统考理综化学试卷(解析版) 题型:选择题
甲醇燃料电池体积小、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用。某甲醇燃料电池的总反应式2CH4O + 3O2= 2CO2+ 4H2O,下图是该燃料电池的示意图。下列说法正确的是
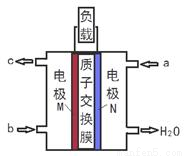
A. a是甲醇燃料、b是氧气
B. 当转移6mole-时,消耗33.6LO2
C. 负极反应:CH4O - 6e- + H2O = CO2↑+ 6H+
D. 质子从N电极区穿过交换膜移向M电极区
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二下学期月考(一)化学试卷(解析版) 题型:填空题
X、Y、Z、W四种元素原子序数依次增大且均小于36。Z基态原子最外层电子数是其内层电子总数的3倍,Y基态原子是同周期元素中未成对电子数最多的原子,X分别与Y、Z元素组合均可形成10电子微粒,W基态原子有10个价电子。 回答下列问题(以下问题均以推知元素符号作答):
(1)若YX3与X2Z、YX2-与ZX-、Y3-与Z2-性质相似,请写出Mg(YX2)2在一定条件下分解的化学反应方程式_________________。
(2)已知X2Z晶胞中X2Z分子的空间排列方式与金刚石晶胞类似,相似的原因与下列因素有关的是______。
①氢键的方向性 ②氢键的饱和性 ③水中氧的杂化方式与金刚石中碳的杂化方式一样 ④晶体类型相似
(3) WZ是一种功能材料,已被广泛用于电池电极、催化剂、半导体、玻璃染色剂等方面。工业上常以W(YZ3)·6X2Z和尿素[CO(NH2)2]为原料制备。
①W2+的基态核外电子排布式为_________,其核外电子有________种运动状态。
②尿素分子中碳原子的杂化方式为_________,1mol尿素分子中含有的σ键数为______NA。
③YZ3-的空间构型________,与之互为等电子体的阴离子如________,中性分子如________;HYZ3与HYZ2 中酸性偏强的是(写化学式)__________。
④WZ晶体的结构与NaCl相同,但天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种WZ晶体中就存在如下图所示的缺陷:一个W2+空缺,另有两个W2+被两个W3+所取代。其结果晶体仍呈电中性,但化合物中W和Z的比值却发生了变化。经测定某样品中W3+与W2+的离子数之比为6:91。若该晶体的化学式为WxZ,则x=_____。
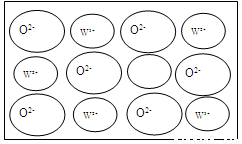
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二下学期月考(一)化学试卷(解析版) 题型:选择题
下列叙述正确的是
A. Ge是IVA族元素, 其核外电子排布式为Ge :[ Ar]4s24p2, 属于P区元素
B. 非极性分子往往是高度对称的分子,比如BF3,PC15,H2O2,CO2这样的分子
C. 有机物固态时都是分子晶体
D. 熔融状态的HgC12不能导电,HgC12的稀溶液有弱的导电能力且可作手术刀的消毒液,从不同角度分类HgC12是一种共价化合物、弱电解质、盐、分子晶体
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省高二下学期月考(一)化学试卷(解析版) 题型:选择题
元素周期表中, 某些主族元素与右下方的主族元素的性质具相似性, 这种规律被称为“对角线规则”。 下列叙述不正确的是
A. Li在N2中燃烧生成Li3N B. Li在空气中燃烧生成Li2O2
C. 可用NaOH 溶液分离 Mg(OH)2和Be(OH)2 D. 硼酸钠溶液显碱性
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广西省桂林市高一下学期开学考化学试卷(解析版) 题型:简答题
烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
(1)烟气脱硫、脱硝的环境意义是______________________;
(2)一种选择性催化脱硝(NO2)的原理为:6NO2+8NH3 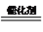 7N2+12H2O
7N2+12H2O
① 上述反应中被还原的元素是_________(填元素符号),反应中每转移3mol电子,生成标准状况下N2的体积为____________;
② 超音速飞机排放的尾气是平流层中NOx的主要来源.它们破坏臭氧层的主要机理为:
Ⅰ 、O3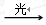 O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
上述反应中NOx所起的作用是_____________;
(3)下表列出了2种燃煤烟气脱硫方法的原理。
方法Ⅰ | 用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4 |
方法Ⅱ | 用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫 |
①方法Ⅰ中用氨水吸收燃煤烟气中的SO2转化为NH4HSO3,是利用了SO2的___________性质(选填字母编号)。
A.漂白性 B.氧化性  C.还原性 D.酸性氧化物
C.还原性 D.酸性氧化物
②方法Ⅰ中氨水吸收燃煤烟气中SO2的化学反应为:2NH3+SO2+H2O=(NH4)2SO3
(NH4)2SO3+SO2+H2O=2NH4HSO3,能提高燃煤烟气中SO2去除率的措施有______(填字母).
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D.通入空气使HSO3-转化为SO42-
③采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的CO2,原因是_________________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高一下学期开学考试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列有关说法正确的是( )
A. 22.4LO2中一定含有NA个氧分子
B. 1mol/LNaCl的溶液中一定含有2NA个离子
C. 2.3g金属钠在足量氧气中充分燃烧,转移0.1NA个电子
D. 4g氦气含有0.5NA个氦分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com