
科目:高中化学 来源:不详 题型:单选题
| A.各物质的浓度不随时间变化 |
| B.容器的压强不再变化 |
| C.B的生成速率和D的生成速率为3:1 |
| D.混合气体的密度不再变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
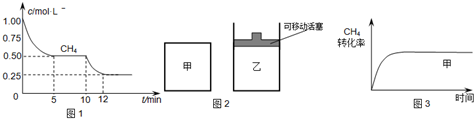
| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
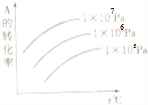
| A.m+n<p+q;Q>0 | B.m+n>p+q;Q>0 |
| C.m+n<p+q;Q<0 | D.m+n>p+q;Q<0 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
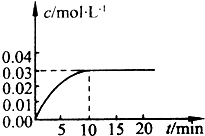
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.2mol SO2+1mol O2 |
| B.4mol SO2+1mol O2 |
| C.2mol SO2+1mol O2+2mol SO3 |
| D.3mol SO2+1mol SO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 高温 |
| 温度 | 25℃~550℃~600℃~700℃ |
| 主要成份 | WO3W2O5WO2W |
| 1400℃ |
| 约3000℃ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.合成氨工作中采用较高的压强 |
| B.硫酸工业生产中,O2与SO2物质的量的比值大于1﹕2 |
| C.将盛有NO2与N2O4混合气体的玻璃球放入热水中,气体颜色加深 |
| D.高温下食品易变质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com