
| 催化剂 |
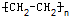 ,
,| 催化剂 |
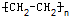 ,加聚反应(或聚合反应);
,加聚反应(或聚合反应); ,
, ,取代反应;
,取代反应;| 醇 |
| △ |
| 醇 |
| △ |


科目:高中化学 来源: 题型:
| A、溶液是电中性的,胶体是带电的 |
| B、两者的分散质微粒均能透过半透膜和滤纸 |
| C、溶液中溶质分子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动 |
| D、一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:C<B |
| B、元素A、C的氧化物均为共价化合物 |
| C、金属性:D>C |
| D、元素B、C、D的最高价氧化物对应水化物能相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素周期表中一共有7个周期和18个族 |
| B、金属元素的原子最外层电子数一定都小于4 |
| C、质量数相同的两种原子,一定不互为同位素 |
| D、主族元素X的原子序数为a,所在周期的元素种数为b,则与x同族的下一周期的元素Y的原于序数一定为a+b |
查看答案和解析>>
科目:高中化学 来源: 题型:
 CuSO4在活化闪锌矿(主要成分是ZnS)方面有重要作用,主要是活化过程中生成CuS、Cu2S等一系列铜的硫化物活化组分.
CuSO4在活化闪锌矿(主要成分是ZnS)方面有重要作用,主要是活化过程中生成CuS、Cu2S等一系列铜的硫化物活化组分.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com