
下列离子方程式中,属于水解反应的是
A.CH3COOH+H2O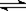 CH3COO-+H3O+ B.CO2+H2O
CH3COO-+H3O+ B.CO2+H2O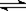 HCO3- +H+
HCO3- +H+
C.CO32-+H2O HCO3-+OH- D.HS-+H2O
HCO3-+OH- D.HS-+H2O S2-+H3O+
S2-+H3O+
科目:高中化学 来源: 题型:
A和甲是来自石油和煤的两种基本化工原料。A是气态烃,甲是液态烃。B和D是生活中两种常见的有机物,F是高分子化合物。相互转化关系如图所示。

(1)A分子的电子式是________;D中官能团名称是________。
(2)在反应①~⑥中,属于加成反应的是________;属于取代反应的是________(填序号)。
(3)B和D反应进行比较缓慢,提高该反应速率的方法
________________________________________________________________________
________________________________________________________________________(填一种即可)
用于鉴别B、D和甲的一种试剂是________。
(4)写出下列反应的化学方程式:
G―→B+E:___________________________________________________;
A―→F:__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关说法中不正确的是( )
A.1 mol氧气中含有1.204×1024个氧原子,在标准状况下的体积约为22.4 L
B.1 mol臭氧和1.5 mol氧气中含有的氧原子数相同
C.等体积、等浓度的醋酸和盐酸电离出的氢离子数之比为1∶1
D.等物质的量的干冰和冰醋酸中所含碳原子数之比为1∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)0.7 mol H2O的质量为 ,
其中含有 个水分子,氢原子的物质的量为_______________________。
(2)质量相同的H2、NH3、SO2、O3四种气体中,含有分子数目最少的是 ,在相同温度和相同压强条件下,体积最大的是 。
(3)2 mol的CO2与3 mol的SO3的分子数比是_______;原子数比是_________。
(4)在9.5 g某二价金属的氯化物中含有0.2 mol Cl-,此氯化物的摩尔质量为____________________,该金属元素的相对原子质量为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,下列有关叙述正确的是
①生成物的百分含量一定增大 ②生成物的产量一定增加 ③反应物的转化率一定增大
④反应物的浓度一定降低 ⑤正反应速率一定大于逆反应速率 ⑥使用了适宜的催化剂
A.② ⑤ B.① ② C.③ ⑤ D.④ ⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
向少量FeCl3溶液中滴入KSCN溶液,发生反应:FeCl3+3KSCN Fe(SCN)3+3KCl。欲使试管内溶液红色变浅,下列措施合理的是
Fe(SCN)3+3KCl。欲使试管内溶液红色变浅,下列措施合理的是
①加Fe(SCN)3 ②加NaOH固体 ③加Zn粉 ④加KCl固体
A.②③ B.②④ C.①② D.①④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )
A.H2O分子和NH3分子具有相同数目的质子总数 B. 18O和O2-是两种不同的核素
C.H O和H
O和H O属于同素异形体 D. 14C和14N互为同位素
O属于同素异形体 D. 14C和14N互为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素A、B、C、D在周期表中的位置如图所示,B、D最外层电子数之和为12,二者可形成DB2、DB3两种分子,DB2具有漂白性。回答下列问题:
| A | B | |
| C | D |
(1)A的氢化物的电子式是 。
(2)下列叙述中,正确的是 (填字母)。
a.稳定性:A的氢化物>C的氢化物 b.还原性:B2->D2-
c.酸性:H4CO4>H2DO4 d.最高化合价:D=B>A>C
(3)DB2通过下列工艺流程可制化工业原料H2DB4和清洁能源H2。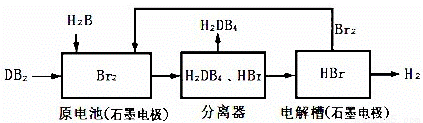
①根据资料:
| 化学式 | Ag2SO4 | AgBr | AgCl |
| Ksp | 1.4×10-5 | 5.0×10-13 | 1.8×10-10 |
为检验分离器的分离效果,取分离后的H2DB4溶液于试管,向其中逐滴加入AgNO3溶液至充分反应,若观察到 ,证明分离效果较好。
②在原电池中,负极发生的反应式为 。
③在电解过程中,电解槽阴极附近溶液pH (填“变大”、“变小”或“不变”)。
④将该工艺流程用总反应的化学方程式表示为: ;该生产工艺的优点有 (答一点即可)。
⑤某含有大量氯化银沉淀的悬浊液中c(Cl-)=0.36mol·L-1,加入等体积的溴化钠溶液,若要产生溴化银沉淀,加入的溴化钠溶液的最小浓度是 mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com