

 ,1mol A完全燃烧消耗9mol O2.
,1mol A完全燃烧消耗9mol O2. .
. 分析 由合成路线可知,反应①为光照条件下的取代反应,所以A为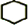 ,反应②为卤代烃发生的消去反应,反应③为环己烯的加成反应,B为
,反应②为卤代烃发生的消去反应,反应③为环己烯的加成反应,B为 ,反应④为卤代烃的消去反应,生成环己二烯,
,反应④为卤代烃的消去反应,生成环己二烯,
(1)由反应①可知,A与氯气在光照的条件下发生取代反应生成一氯环己烷,故A为 ;根据A的分子式计算出1molA完全燃烧消耗氧气的物质的量;
;根据A的分子式计算出1molA完全燃烧消耗氧气的物质的量;
(2)由转化关系可知,反应②由一氯环己烷去掉HCl生成环己烯;
(3)由合成路线可知,B为1,2-二溴环己烷,故反应④是1,2-二溴环己烷发生消去反应生成1,4-环己二烯.
解答 解:由合成路线可知,反应①为光照条件下的取代反应,所以A为 ,反应②为卤代烃发生的消去反应,反应③为环己烯的加成反应,B为
,反应②为卤代烃发生的消去反应,反应③为环己烯的加成反应,B为 ,反应④为卤代烃的消去反应,生成环己二烯,
,反应④为卤代烃的消去反应,生成环己二烯,
(1)由反应①可知,A与氯气在光照的条件下发生取代反应生成一氯环己烷,故A为 ,为环己烷,环己烷的分子式为C6H12,1mol环己烷完全燃烧消耗氧气的物质的量为:(6+$\frac{12}{4}$)mol=9mol,
,为环己烷,环己烷的分子式为C6H12,1mol环己烷完全燃烧消耗氧气的物质的量为:(6+$\frac{12}{4}$)mol=9mol,
故答案为: ;9;
;9;
(2)由转化关系可知,反应②由一氯环己烷去掉HCl生成环己烯,该反应属于消去反应;
故答案为:消去反应;
(3)由合成路线可知,B为1,2-二溴环己烷,故反应④是1,2-二溴环己烷发生消去反应生成1,4-环己二烯,反应条件为氢氧化钠醇溶液加热,反应方程式为 .
.
故答案为: .
.
点评 本题考查有机物的合成,为高频考点,题目难度中等,明确反应条件与反应类型的关系来推出各物质是解答本题的关键,注意卤代烃的水解、消去反应的条件.


科目:高中化学 来源: 题型:选择题
| A. | 1mol | B. | 1.6mol | C. | 2.2mol | D. | 2.4mol |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 近年来全国各地长期被雾霾笼罩,雾霾颗粒中汽车尾气占20%以上.已知汽车尾气中的主要污染物为NOx、CO、燃烧源超细颗粒(PM2.5)等由害物质.目前,已研究出了多种消除汽车尾气污染的方法.
近年来全国各地长期被雾霾笼罩,雾霾颗粒中汽车尾气占20%以上.已知汽车尾气中的主要污染物为NOx、CO、燃烧源超细颗粒(PM2.5)等由害物质.目前,已研究出了多种消除汽车尾气污染的方法.
| 实验编号 | 温度/°C | 起始时NO的物质的量/mol | 平衡时N2的物质的量/mol |
| 1 | 700 | 0.40 | 0.09 |
| 2 | 800 | 0.24 | 0.08 |
| 3 | 800 | 0.20 | a |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海带、紫菜等海藻类植物中含有丰富的I2 | |
| B. | 灼烧海带样品时,坩埚应该垫在石棉网上加热 | |
| C. | 可以用CCl4、裂化汽油等有机溶剂把碘萃取出来 | |
| D. | 分液漏斗中液体的总体积不得超过其容量的$\frac{2}{3}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| t(s) | 0 | 500 | 1000 | 1500 |
| n(NO2)(mol) | 20 | 13.96 | 10.08 | 10.08 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 ,B中含有的化学键类型是离子键、共价键.
,B中含有的化学键类型是离子键、共价键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | BaCl2溶液 | B. | 稀盐酸、BaCl2溶液 | ||
| C. | 稀硝酸、BaCl2溶液 | D. | 稀硫酸、BaCl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com