
| 阳离子 | Na+Mg2+Al3+Ag+Ba2+ |
| 阴离子 | OH- Cl- SO42- CO32- |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 常温下有浓度为0.1mol/L、体积为V L的氨水,向其中逐滴加入一定浓度的盐酸,得到如图的滴定曲线,其中d点时两种溶液恰好完全反应.根据图象回答下列问题:
常温下有浓度为0.1mol/L、体积为V L的氨水,向其中逐滴加入一定浓度的盐酸,得到如图的滴定曲线,其中d点时两种溶液恰好完全反应.根据图象回答下列问题:| c(H+) |
| c(OH-) |
| c(NH4+)?c(OH-) |
| c(NH3?H2O) |
| c(NH3?H2O) |
| c(NH4+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
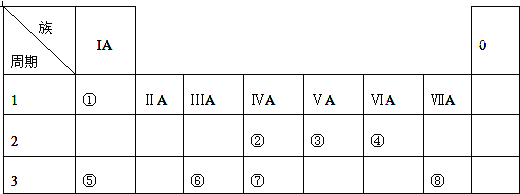
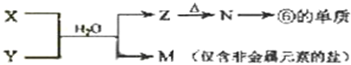
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaCl、BaSO4、SO2 |
| B、Cu、CH3COOH、酒精 |
| C、KNO3、NH3?H2O、Cl2 |
| D、CaCO3、H2O、液氨 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、正常雨水的pH为7.0,酸雨的pH小于7.0 |
| B、严格执行机动车尾气排放标准有利于防止大气污染 |
| C、食品厂产生的含丰富氮、磷营养素的废水可长期排向水库养鱼 |
| D、使用氯气对自来水消毒过程中,生成的有机氯化物可能对人体有害 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com