
(12分)已知固体草酸(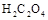 )分解的化学方程式为:
)分解的化学方程式为:
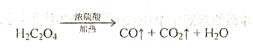
某实验小组为测定铁锈样品的组成(假定铁锈中只有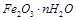 和
和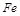 两种成份),利用草酸分解产生的CO和铁锈反应,实验装置如下图所示。
两种成份),利用草酸分解产生的CO和铁锈反应,实验装置如下图所示。
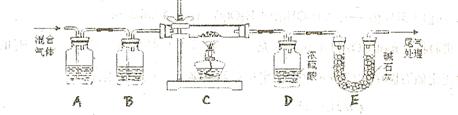
(1)为得到干燥、纯净的CO气体,洗气瓶A、B中盛放的液态试剂依次是 、 (填答案编号)a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液 d.氯化钙溶液
(2)在点燃C处酒精灯之前应进行的操作是:(a)检查装置气密性;
(b) ;
(3)E装置的作用是 。
上述装置最后尾气处理的方法是 :
(4)准确称量样品质量10.00g置于硬质玻璃管中,充分反应后冷却、称量(假设每步均完全反应),硬质玻璃管中剩余固体质量为8.32g,D中浓硫酸增重0.72g,则n= .
(5)在本实验中,下列情况会使测定结果n偏大的是 (填答案编号)
a.缺少装置B b.缺少装置E c.反应后的固体剩余少量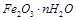
科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:2012-2013学年湖北省八校高三第一次联考(12月)理综化学试卷(解析版) 题型:填空题
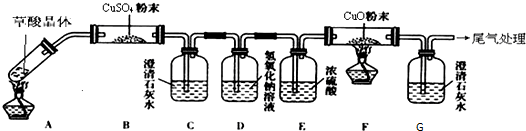
将1.000gFeC2O4·2H20固体样品放在热重分析仪中进行热重分析,測得其热重分析曲线(样品质量随温度变化的曲线)如下图所示:
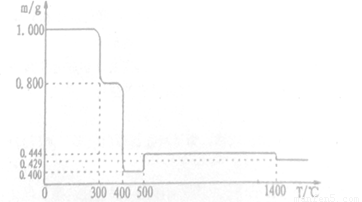
已知:①草酸盐受热分解易放出碳的氧化物。②5000C之前,该热重分析仪的样品池处于 Ar气气氛中,5000C时起,样品池与大气相通。完成下列填空:
(1) 3000C时是样品脱水的过程,试确定3500C时样品是否脱水完全_____ (填“是"或 否“),判断的理由是____(要求写出推算过程)。
(2 ) 4000C时发生变化的化学方程式是_______。
(3) 将6000C 时样品池中残留的固体隔绝空气冷却至室温,再向该固体中加入一定量的稀盐酸刚好完全溶解,用pH试纸测得所得溶液的PH=3,其原因是____(用离子方程式回答):向该溶液中滴加适量NaOH溶液生成红褐色沉淀,測得此时溶液中铁元索的离子浓度为4.0x10-11 mol/L,则此时溶液的pH= _______(已知:Ksp[Fe(OH)2]=8.0×10-16,Ksp[Fe(OH)3]=4.0×10-38)
(4) 将15000C时样品池中残留的固体隔绝空气冷却后,用稀盐酸溶解得一棕黄色溶液。 取少量该溶液滴加KSCN,溶液显红色;另取少量该溶液滴加K3[Fe(CN)6)(铁氰化钾)溶液,产生特征蓝色沉淀。试写出图中14000C时发生反应的化学方程式_________ ,产生特征蓝色沉淀的离子反应方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)已知固体草酸(![]() )分解的化学方程式为:
)分解的化学方程式为:
某实验小组为测定铁锈样品的组成(假定铁锈中只有![]() 和
和![]() 两种成份),利用草酸分解产生的CO和铁锈反应,实验装置如下图所示。
两种成份),利用草酸分解产生的CO和铁锈反应,实验装置如下图所示。
(1)为得到干燥、纯净的CO气体,洗气瓶A、B中盛放的液态试剂依次是 、 (填答案编号)a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液 d.氯化钙溶液
(2)在点燃C处酒精灯之前应进行的操作是:(a)检查装置气密性;
(b) ;
(3)E装置的作用是 。
上述装置最后尾气处理的方法是 :
(4)准确称量样品质量10.00g置于硬质玻璃管中,充分反应后冷却、称量(假设每步均完全反应),硬质玻璃管中剩余固体质量为8.32g,D中浓硫酸增重0.72g,则n= .
(5)在本实验中,下列情况会使测定结果n偏大的是 (填答案编号)
a.缺少装置B b.缺少装置E c.反应后的固体剩余少量![]()
查看答案和解析>>
科目:高中化学 来源:2012届山东省实验中学高三第三次诊断性测试化学试卷 题型:填空题
(12分)已知固体草酸(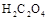 )分解的化学方程式为:
)分解的化学方程式为: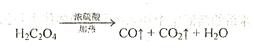
某实验小组为测定铁锈样品的组成(假定铁锈中只有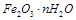 和
和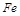 两种成份),利用草酸分解产生的CO和铁锈反应,实验装置如下图所示。
两种成份),利用草酸分解产生的CO和铁锈反应,实验装置如下图所示。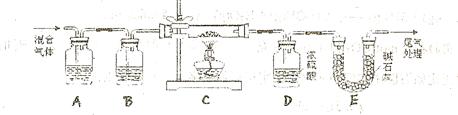
(1)为得到干燥、纯净的CO气体,洗气瓶A、B中盛放的液态试剂依次是 、 (填答案编号)a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液 d.氯化钙溶液
(2)在点燃C处酒精灯之前应进行的操作是:(a)检查装置气密性;
(b) ;
(3)E装置的作用是 。
上述装置最后尾气处理的方法是 :
(4)准确称量样品质量10.00g置于硬质玻璃管中,充分反应后冷却、称量(假设每步均完全反应),硬质玻璃管中剩余固体质量为8.32g,D中浓硫酸增重0.72g,则n= .
(5)在本实验中,下列情况会使测定结果n偏大的是 (填答案编号)
a.缺少装置B b.缺少装置E c.反应后的固体剩余少量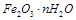
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com