
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源:不详 题型:单选题
 2SO3在一定条件下达到化学反应的限度时( )
2SO3在一定条件下达到化学反应的限度时( )| A.①② | B.①③ | C.只有③ | D.只有① |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.熵值是一个物理量,只与物质的种类有关,而与其它因素无关 |
| B.同一种物质,其所处的状态不同,熵值不同 |
| C.不同种物质,同一状态(T、P)下,熵值不同 |
| D.同一物质,当物质的量一定时,温度越高,熵值越大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.放热反应一定是自发进行的反应 |
| B.吸热反应一定是非自发进行的反应 |
| C.自发反应在恰当的条件下才能自发 |
| D.凡是放热反应都是自发的,由于吸热反应都是非自发的 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X2为0.2mol/L | B.Y2为0.2mol/L |
| C.Z2为0.4mol/L | D.Y2为0.6mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe3O4+4CO═3Fe+4CO2/△H=-14kJ?mol-1 |
| B.Fe3O4(s)+4CO(g)═3Fe(s)+4CO2(g)△H=-22kJ?mol-1 |
| C.Fe3O4(s)+4CO(g)═3Fe(s)+4CO2(g)△H=+14kJ?mol-1 |
| D.Fe3O4(s)+4CO(g)═3Fe(s)+4CO2(g)△H=-14kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2 SO3(g);△H<0。某研究小组进行了当其他条件不变时,改变某一条件对上述反应影响的研究,下列分析正确的是
2 SO3(g);△H<0。某研究小组进行了当其他条件不变时,改变某一条件对上述反应影响的研究,下列分析正确的是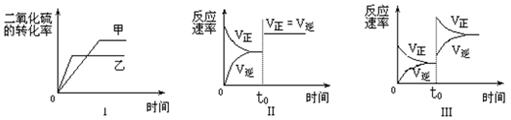
| A.①② | B.②③ | C.②④ | D.③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com