
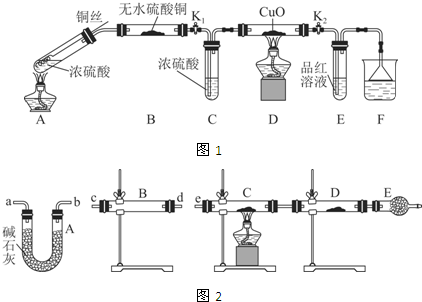
| 装置 | 所盛药品 | 实验现象 | 结论或解释 |
| B | ① | ② | ③ |
| C | CuO固体 | ④ | ⑤ |
分析 Ⅰ.(1)铜与浓硫酸加热反应生成硫酸铜、二氧化硫气体和水,据此写出反应的化学方程式;
(2)二氧化硫有毒,多余的二氧化硫气体需要用氢氧化钠溶液或酸性高锰酸钾溶液吸收;
(3)根据C中氧化铜是否被还原及E中品红溶液是否褪色判断;
(4)反应后的混合液中含有浓硫酸,不能向冷却后的溶液中加水,否则会导致液体溅出,应该类比稀释浓硫酸的方法进行操作;
Ⅱ.(1)随着反应的进行浓硫酸被消耗会变成稀硫酸,锌与稀硫酸反应产生氢气,所以SO2中的杂质可能为H2和H2O(g);
(2)检验H2的方法常用灼热的CuO反应生成水,检验水的存在,这里有水蒸气的存在,注意操作的顺序,先检验水的存在,将水除尽,再检验H2和CuO反应生成的水;
(3)实验先检验是否含有水,利用无水硫酸铜吸水变蓝色检验;将水除尽,再检验H2和CuO反应生成的水.
解答 解:Ⅰ.(1)碳和浓硫酸在加热条件下生成二氧化碳、二氧化硫和水,反应的化学方程式为:2H2SO4(浓)+Cu$\frac{\underline{\;\;△\;\;}}{\;}$SO2↑+SO42-+Cu2++2H2O,
故答案为:2H2SO4(浓)+Cu$\frac{\underline{\;\;△\;\;}}{\;}$SO2↑+SO42-+Cu2++2H2O;
(2)二氧化硫气体是一种有毒气体,剩余的二氧化硫气体不能直接排放,应该用NaOH溶液或酸性KMnO4溶液等吸收,
故答案为:NaOH溶液(或酸性KMnO4溶液等);
(3)由于D装置中黑色固体颜色无变化,E中溶液褪色,说明反应生成了二氧化硫,证明反应中S元素被还原,在反应中作氧化剂,而氢离子没有被还原,所以浓硫酸的中S的氧化性大于氢离子,
故答案为:D装置中黑色固体颜色无变化,E中溶液褪色;
(4)含有铜离子的溶液显示蓝色,需要将反应后的溶液用水稀释,由于反应后的溶液中含有浓硫酸,所以应该将A装置中试管内冷却的混合物沿杯壁(或玻璃棒)缓缓倒入盛有水的烧杯中,并不断搅拌,看溶液是否变蓝,
故答案为:将A装置中试管内冷却的混合物沿杯壁(或玻璃棒)缓缓倒入盛有水的烧杯中,并不断搅拌,看溶液是否变蓝;
Ⅱ.(1)随着反应的进行浓硫酸被消耗会变成稀硫酸,锌与稀硫酸反应产生氢气,所以SO2中的杂质可能为H2和H2O(g),
故答案为:氢气和水蒸气;
(3)先检验水的存在,将水除尽,再检验H2和CuO反应生成的水,B装置检验水,A装置除去气体中的水蒸气,C、D用于检验气体中是否含有H2,所以气流方向为:c d(或d c)a b(或b a)e,
故答案为:c d(或d c)a b(或b a)e;
(4)B装置检验水,装置内盛放无水硫酸铜,若固体由白色变成蓝色,说明SO2中含有水蒸气;
若含有H2,在装置C中发生反应H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,固体由黑色变成红色,D装置内固体由白色变成蓝色,说明SO2中含有氢气,
故答案为:
| 装置 | 所盛药品 | 实验现象 | 结论或解释 |
| B | 无水硫酸铜 | 固体由白色变成蓝色 | SO2中含有水蒸气 |
| C | C装置中固体由黑色变成红色,D装置内固体由白色变成蓝色 | SO2中含有氢气 |
点评 本题考查了浓硫酸的性质、常见气体检验的方法和操作顺序、对实验原理的理解等,题目难度中等,注意掌握浓硫酸的性质及常见气体的检验方法,Ⅱ(3)中要检验SO2中是否含有H2和H2O(g),需要注意检验的顺序,应该先检验水,然后除去二氧化硫后再检验氢气.


科目:高中化学 来源: 题型:选择题
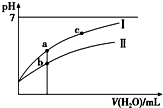 已知:25℃时某些弱酸的电离平衡常数(如表).下面图象表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.下列说法正确的是( )
已知:25℃时某些弱酸的电离平衡常数(如表).下面图象表示常温下,稀释CH3COOH、HClO两种酸的稀溶液时,溶液pH随加水量的变化.下列说法正确的是( ) | CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
| A. | 相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | 向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O═2HClO+CO32- | |
| C. | 图象中a、c两点处的溶液中$\frac{c({R}^{-})}{c(HR)•c(O{H}^{-})}$相等(HR代表CH3COOH或HClO) | |
| D. | 图象中a点酸的总浓度大于b点酸的总浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 操作II中,通入硫化氢至饱和的目的是使Sn2+转化为SnS沉淀并防止Fe2+被氧化 | |
| B. | 在溶液中用硫酸酸化至pH=2的目的防止Fe2+沉淀 | |
| C. | 操作Ⅰ所得滤液中可能含有Fe3+ | |
| D. | 常用标准KMnO4溶液滴定的方法测定绿矾产品中Fe2+的含量,滴定时发生反应的离子方程式为:5Fe2++MnO4-+8H+→5Fe3++Mn2++4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
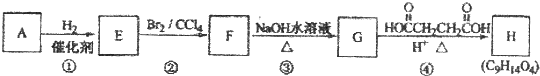
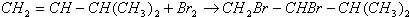 ;
;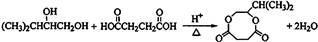 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 无色溶液中滴加氯水和CCl4,振荡、静置 | 上层溶液显紫色 | 原溶液中有I- |
| B | 将SO2通入酸性KMnO4溶液中 | 紫色褪去 | SO2具有还原性 |
| C | 向明矾溶液中通入过量氨气 | 先产生大量白色沉淀,后沉淀逐渐消失 | Al(OH)3能溶于氨水 |
| D | AgI沉淀中滴入浓KCl溶液 | 有白色沉淀出现 | 溶解度:AgCl<AgI |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
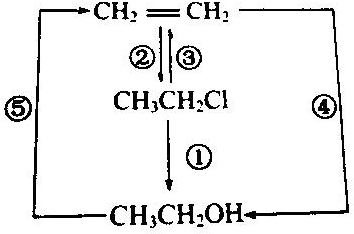
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com