
| A. | Ag2O 被还原,是负极材料 | |
| B. | 正极增重16 克时电路中有2NA个电子转移 | |
| C. | 用该电池进行电解水试验,每生成标况下aLO2,电池负极增重16a/11.2 克 | |
| D. | 该电池的电解质溶液显酸性 |
分析 根据电池的电极反应式为:Zn+Ag2O=ZnO+2Ag知,Zn失电子化合价升高为负极、Ag2O作正极,放电时,负极上消耗氢氧根离子、正极上生成氢氧根离子,根据电极反应结合电子守恒分析解答.
解答 解:根据电池的电极反应式为:Zn+Ag2O=ZnO+2Ag知,Zn失电子化合价升高为负极、Ag2O作正极,放电时,该电池的负极反应式为:Zn+2OH--2e-═Zn(OH)2,正极上:Ag2O+H2O+2e-═2Ag+2OH-.
A、Ag2O 被还原,是正极材料,故A错误;
B、正极反应:Ag2O+H2O+2e-═2Ag+2OH-.正极质量会减轻,故B错误;
C、用该电池进行电解水试验,根据反应:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,每生成标况下1molO2,转移电子4mol,该电池的负极反应式为:Zn+2OH--2e-═Zn(OH)2,转移2mol电子,电池的负极增重34g,所以每生成标况下aLO2,电池负极增重16a/11.2 克,故C正确;
D、该电池的电解质溶液不能显酸性,否则氧化性不能产生存在,故D错误.
故选C.
点评 本题考查了原电池原理,根据电极反应式中元素化合价变化确定正负极,再结合离子移动方向、正负极上发生的反应分析解答,题目难度不大.


科目:高中化学 来源: 题型:推断题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10℃20mL 3mol/L的X溶液 | B. | 20℃10mL 4mol/L的X溶液 | ||
| C. | 20℃30mL 2mol/L的X溶液 | D. | 10℃10mL 2mol/L的X溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应中氧化剂是C12 | B. | 每有1mol C12反应转移1mole- | ||
| C. | 反应中S元素的价态降低 | D. | 该反应中H2O被氧化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe和盐酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 硫酸与氢氧化钡溶液反应:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| C. | Cu和AgNO3溶液反应:Cu+Ag+═Cu2++Ag | |
| D. | 石灰石和盐酸反应:CaCO3+2H+═Ca2++CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  2-乙基丁烷 2-乙基丁烷 | B. | CH3CHBr2二溴乙烷 | ||
| C. |  2-甲基丁烯 2-甲基丁烯 | D. | 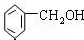 苯甲醇 苯甲醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 18O 31P 35Cl | B. | 27Al 19F 12C | ||
| C. | 第一周期所有元素的原子 | D. | 元素周期表中ⅤA所有元素的原子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com