
| A. | 漂白粉和明矾都常用于自来水的处理,且二者的作用原理相同 | |
| B. | Na的还原性比Cu强,故可用Na与CuSO4溶液反应制取Cu | |
| C. | 不能用带玻璃塞的玻璃瓶盛放碱液 | |
| D. | 玻璃、水泥、陶瓷、水晶都是重要的硅酸盐材料 |
分析 A.漂白粉生成具有强氧化性的次氯酸,明矾水解生成具有吸附性的氢氧化铝;
B.钠与硫酸铜溶液反应实质是先与水反应生成氢氧化钠,氢氧化钠再与硫酸铜反应生成硫酸钠和氢氧化铜沉淀;
C.玻璃中的二氧化硅与氢氧化钠溶液反应生成具有硅酸钠溶液;
D.水晶主要成分为二氧化硅.
解答 解:A.漂白粉生成具有强氧化性的次氯酸,明矾水解生成具有吸附性的氢氧化铝,二者原理不同,故A错误;
B.Na的还原性比Cu强,但是Na与CuSO4溶液反应生成氢氧化铜、硫酸钠和水,得不到Cu,故B错误;
C.玻璃中的二氧化硅与氢氧化钠溶液反应生成具有硅酸钠溶液,能够将玻璃塞与玻璃瓶粘到一起,故C正确;
D.水晶主要成分为二氧化硅,是氧化物,不属于硅酸盐,故D错误;
故选:C.
点评 本题考查较为综合,多角度考查元素混合物知识,明确相关物质的性质是解题关键,有利于培养学生良好的科学素养,提高学习的积极性,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | Fe2O3 | B. | Fe3O4 | C. | Fe4O5 | D. | Fe5O7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在pH=1的溶液中:NH4+、K+、ClO-、Cl- | |
| B. | 水电离的c(H+)=1.0×10-13mol•L-1的溶液中:Na+、Mg2+、Ca2+、I- | |
| C. | 有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br- | |
| D. | 在c(H+)=1.0×10-13mol•L-1的溶液中:Na+、S2-、AlO2-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在含等物质的量的FeBr2、FeI2的溶液中缓慢通入Cl2:I-、Fe2+、Br- | |
| B. | 在含等物质的量的Fe3+、Cu2+、H+的溶液中加入Zn:H+、Fe3+、Cu2+、Fe2+ | |
| C. | 在含等物质的量的Ba(OH)2、KOH的溶液中通入CO2:Ba(OH)2、KOH、BaCO3、K2CO3 | |
| D. | 在含等物质的量的AlO2-、OH-、CO32-溶液中,逐滴加入盐酸:OH-、CO32-、AlO2-、Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子半径:Y<Z<W | |
| B. | Z分别与X、Y形成的化合物中,化学键类型均相同 | |
| C. | X分别与Y、W形成的最简单化合物的稳定性:W<Y | |
| D. | 由以上四种元素形成的化合物一定能促进水的电离 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解精炼粗铜时,粗铜应作阴极 | |
| B. | 氯碱工业的阳极区得到的产品是H2和NaOH | |
| C. | 将金属与直流电源的负极相连的方法叫做外加电流的阴极保护法 | |
| D. | 同种金属作为原电池的正极比作为电解池的阳极腐蚀得更快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平衡后向容器中再充入与初始投料相同物质的量的CO2和H2,则CO的平衡浓度变为原来的2倍 | |
| B. | 恒温恒容下,增大压强,H2的浓度一定减小 | |
| C. | 升高温度,逆反应速率减小 | |
| D. | 该反应化学方程式为:CO2(g)+H2(g)?CO(g)+H2O(g)△H<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 | |
| B. | 硫酸铁易溶于水,可作净水剂 | |
| C. | 我国首艘航母“辽宁舰”上用于舰载机降落的拦阻索是特种钢缆,属于金属材料 | |
| D. | 减少烟花爆竹的燃放,有利于降低空气中的PM2.5含量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
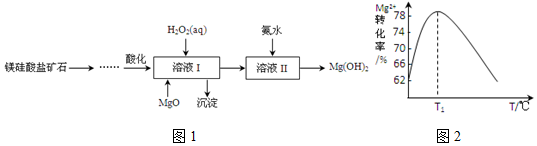
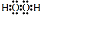 .溶液 I中加入H2O2溶液发生反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.
.溶液 I中加入H2O2溶液发生反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com