
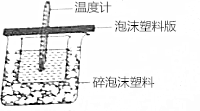
 某实验小组设计用0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于如图所示的装置中进行测定中和热的实验.
某实验小组设计用0.55mol/L的NaOH溶液50mL与0.50mol/L的盐酸50mL置于如图所示的装置中进行测定中和热的实验.分析 (1)根据量热计的构造来判断该装置的缺少仪器;为了减少热量的损失,大烧杯杯口与小烧杯杯口相平,两烧杯之间塞满碎泡沫塑料;大烧杯上如不盖硬纸板,会使一部分热量散失;
(2)为了确保定量的HCl反应完全,所用NaOH稍过量;
(3)没有用水洗涤温度计上的盐酸溶液,导致盐酸的物质的量偏小,放出的热量偏小;温度计上的碱未用水冲洗,因碱是过量的,放出的热量不变.
解答 解:(1)由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌器;为了减少热量的损失,大烧杯杯口与小烧杯杯口相平,两烧杯之间塞满碎泡沫塑料;大烧杯上如不盖硬纸板,会使一部分热量散失,求得的中和热数值将会减小,
故答案为:环形玻璃搅拌器;大烧杯杯口与小烧杯杯口没有相平,两烧杯之间没有塞满碎泡沫塑料;偏小;
(2)实验中,所用NaOH稍过量的原因是确保定量的HCl反应完全;
故答案为:确保定量的HCl反应完全;
(3)没有用水洗涤温度计上的盐酸溶液,导致盐酸的物质的量偏小,放出的热量偏小,测得的中和热数值偏小;温度计上的碱未用水冲洗,因碱是过量的,放出的热量不变,对测定结果无影响;
故答案为:偏小;无影响.
点评 本题考查了中和热的测定方法,题目难度中等,明确中和热的测定原理为解答关键,注意掌握中和热计算方法,试题培养了学生的分析能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | NaCl的摩尔质量是58.5 g | |
| B. | 0.5 mol CO2气体中所含的CO2分子数约为3.01×1023 | |
| C. | 标准状况下,6.02×1022个CO2分子所占的体积约是22.4 L | |
| D. | 在1 L水中溶解5.85g NaCl,即可配制得0.1 mol•L-1的NaCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
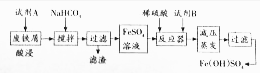
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
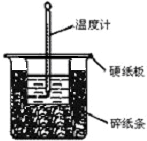 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:| 温度 序号 | 起始温度t1/℃ | 终止温度 T2/℃ | 温度差 △t/℃ | ||
| HCl | NaOH | 平均值 | |||
| 1 | 25 | 25 | 27.3 | ||
| 2 | 25 | 25 | 27.4 | ||
| 3 | 25 | 25 | 28.6 | ||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 图为金的晶胞结构示意图,若金的原子半径为r,则空间利用率的表达式为( )(金的相对原子质量为197)
图为金的晶胞结构示意图,若金的原子半径为r,则空间利用率的表达式为( )(金的相对原子质量为197)| A. | $\frac{{\frac{4}{3}π{r^3}×4}}{{{{({\frac{4}{{\sqrt{2}}}r})}^3}}}$×100% | B. | $\frac{{\frac{4}{3}π{r^3}×14}}{{{{({\frac{4}{{\sqrt{2}}}r})}^3}}}$×100% | ||
| C. | $\frac{{\frac{197}{NA}×4}}{{{{({\frac{4}{{\sqrt{2}}}r})}^3}}}$×100% | D. | $\frac{{\frac{4}{3}π{r^3}×8}}{{{{({\frac{8}{{\sqrt{3}}}r})}^3}}}$×100% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(SiF4)消耗=4v(HF)生成 | B. | HF的体积分数不再变化 | ||
| C. | 容器内气体压强不再变化 | D. | 容器内气体的总质量不再变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com