
如图所示是17世纪炼金家们画的带有浓厚神秘色彩的两种同族元素的元系符号。已知X位于周期表前四周期,Y比X多1个电子层,X、Y都是生产半导体的材料,X的氢化物XH3有剧毒。下列推测不正确的是( )

A.原子半径X<Y
B.最高价氧化物对应的水化物酸性X>Y
C.X的氢化物具有强还原性
D.Y与碘同周期,Y的最高价氧化物对应的水化物的酸性比高碘酸(HIO4)强
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
过氧乙酸是在抗SARS病毒期间常使用的一种高效杀毒剂,其分子式为C2H4O3,它具有氧化性,漂白作用,下列物质中漂白作用原理与过氧乙酸不同的是( )
A.氯水(次氯酸) B.臭氧 C.活性炭 D.过氧化钠
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C为三种短周期元素,A、B同周期,A、C最低价离子分别为A2-、C-,其离子半径A2->C-。B2+与C-具有相同的电子层结构,下列叙述一定不正确的是( )
A.它们的原子序数A>B>C
B.它们的原子半径C>B>A
C.离子半径A2->C->B2+
D.原子核外最外层上的电子数C>A>B
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关元素的性质及其递变规律正确的是( )
A.IA族与VIIA族元素间可形成共价化合物或离子化合物
B.第二周期元素从左到右,最高正价从+1递增到+7
C.同主族元素的简单阴离子还原性越强,水解程度越大
D.同周期金属元素的化合价越高,其原子失电子能力越强
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y和Z均为短周期元素,原子序数依次增大,X的单质为密度最小的气体,Y原子最外层电子数是其周期数的三倍,Z与X原子最处层电子数相同。回答下列问题:
(1)X、Y和Z的元素符号分别为 、 、 。
(2)由上述元素组成的化合物中,既含有共价键又含有离子键的有 、 。
(3)X和Y组成的化合物中,既含有极性共价键又含有非极性共价键的是 。
此化合物在酸性条件下与高锰酸钾反应的离子方程式为  ;此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为 。
;此化合物还可将碱性工业废水中的CN-氧化为碳酸盐和氨,相应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.P和S属于第三周期元素,P原子半径比S小
B.同周期ⅡA和ⅢA族元素的原子序数都相差1
C.短周期元素的离子aA2+、bB+、cC3-、dD-都具有相同的电子层结构,则原子序数、原子半径和单质的还原性都按照A、B、C、D的顺序减小
D.Cl和Br属于第ⅦA族元素,HClO4酸性比HBrO4强。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列热化学方程式中,正确的是( )
A.甲烷的燃烧热为890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B.500℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)2NH3(g) ΔH=-38.6 k J·mol-1
J·mol-1
C.HCl和NaOH反应的中和热为-57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3 kJ·mol-1)
D.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式为2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
我国科学家研制出一中催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:
HCHO+O2 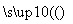 CO2+H2O。下列有关说法正确的是
CO2+H2O。下列有关说法正确的是
A.该反应为吸热反应
B.CO2分子中的化学键为非极性键
C.HCHO分子中既含σ键又含π键
D.每生成1.8gH2O消耗2.24L O2
查看答案和解析>>
科目:高中化学 来源: 题型:
KClO3分解时尚有副反应,导致收集到的气体有异味.据推测,副产物可能是O3、Cl2、ClO2中的一种或几种.资料表明:O3、Cl2、ClO2的沸点依次为﹣111℃、﹣34℃和11℃,且O3、ClO2也能将KI氧化为I2.为探究副反应气体产物的成分,将KClO3分解产生的气体经干燥后通入如装置进行实验:
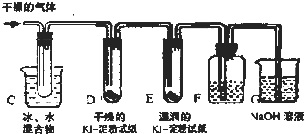
(1)若要确认副产物中含Cl2,F中应盛放 溶液.
(2)确定副产物中含有ClO2的现象是 .
(3)实验时若D中无现象,E中试纸变蓝,能否得出副产物含有臭氧的结论?
答: (填“能”或“不能”).理由是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com