
分析 (1)利用盖斯定律解答,从待求反应出发,分析待求反应中的反应物和生成物在已知反应中的位置,通过相互加减可得,据盖斯定律(①+②)×$\frac{1}{3}$得到;
(2)①从还原剂的概念出发分析反应物的价态变化即可;
②从价态变化出发分析得失电子总数解答;
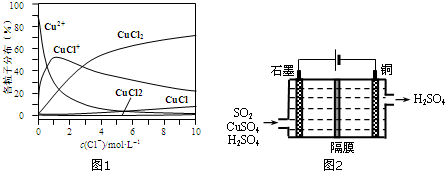
(3)①从图上在c(Cl-)=9mol•L-1处,做一条平行与纵轴的虚线,可以比较;
②从图上在c(Cl-)=1mol•L-1处,做一条平行与纵轴的虚线,看哪种微粒最多;
(4)①二氧化硫是一种有毒的气体,排放到空气中可引起酸雨的发生,对环境和人类健康有害,脱硫可以防止酸雨的发生;
②利用电解原理将二氧化硫转化成硫酸吸收,先写出两个电极上上发生的电极反应式,加和就可得到总的离子方程式.
解答 解:(1)①2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-768.2kJ•mol-1,
②2Cu2O(s)+Cu2S(s)═6Cu(s)+SO2(g)△H=+116.0kJ•mol-1,
据盖斯定律(①+②)×$\frac{1}{3}$得:Cu2S(s)+O2(g)═2Cu(s)+SO2(g)△H=-217.4KJ/mol,
故答案为:-217.4;
(2)①从反应4CuSO4+3H3PO2+6H2O=4CuH↓+4H2SO4+3H3PO4分析,Cu从+2价变成+1,H从+1价变成-1价,P从+1价变成+5价,还原剂化合价升高,故该反应的还原剂是H3PO2,故答案为:H3PO2;
②Cu从+2价变成+1,4molCu得到4mol电子,H从+1价变成-1价,4mol-1价的H得到8mol电子,共得电子12mol,即每生成4molCuH转移电子12mol,所以每生成1molCuH,转移电子3mol电子,
故答案为:1;
(3)①在c(Cl-)=9mol•L-1处,做一条平行与纵轴的虚线,可见溶液中主要含铜物种浓度大小关系为:c(CuCl2)>c(CuCl+)>c(CuCl3-)>c(Cu2+)>c(CuCl42-),
故答案为:c(CuCl2)>c(CuCl+)>c(CuCl3-);
②从图上可见,在c(Cl-)=1mol•L-1的氯化铜溶液中,主要是Cu2+与Cl-结合生成CuCl+,滴入硝酸银溶液发生反应的方程式为:CuCl++Ag+=AgCl↓+Cu2+(CuCl2+Ag+=CuCl++AgCl↓;CuCl2+2Ag+=Cu2++2AgCl↓)
故答案为:CuCl++Ag+=AgCl↓+Cu2+(CuCl2+Ag+=CuCl++AgCl↓;CuCl2+2Ag+=Cu2++2AgCl↓);
(4)①脱硫可以减少二氧化硫的排放量,防止酸雨的发生;
故答案为:防止酸雨的发生;
②分析图中电解装置,可知左边石墨是电解池的阳极,右边是阴极;阳极放电的物质二氧化硫,失去电子生成硫酸根离子,电极反应式:SO2-2e-+2H2O=SO42-+2H+;阴极放电的物质时铜离子,得到电子被还原成单质铜,电极反应式:Cu2++2e-=Cu;将上述两电极的电极反应式得:SO2+2H2O+Cu2+$\frac{\underline{\;通电\;}}{\;}$4H++SO42-+Cu,
故答案为:SO2+2H2O+Cu2+$\frac{\underline{\;通电\;}}{\;}$4H++SO42-+Cu.
点评 本题考查了反应热的求算,盖斯定律,二氧化硫的污染和治理,电解原理,题目综合性强,难度中等,根据已经掌握的知识可以求解,掌握基础是关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
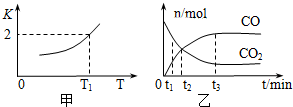 氮、碳都是重要的非金属元素,含氮、碳元素的物质在工业生产中有重要的应用.
氮、碳都是重要的非金属元素,含氮、碳元素的物质在工业生产中有重要的应用.| 容器 | 起始投入 | 达平衡时 | |||
| 甲 | 2mol N2 | 3mol H2 | 0mol NH3 | 1.5mol NH3 | 同种物质的体积分数相同 |
| 乙 | a mol N2 | b mol H2 | 0mol NH3 | 1.2mol NH3 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在豆浆中加入盐卤做豆腐 | |
| B. | 在河流入海处易形成沙洲 | |
| C. | 往红褐色的氢氧化铁胶体中加入过量稀盐酸,溶液变黄色 | |
| D. | 肾衰竭等疾病引起的血液中毒,可利用血液透析进行治疗 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com