
| 操作 | 实验现象 | 结论 | |
| A | 将铝片放入盐酸中 | 产生气泡的速率开始时较慢,随后加快,后来又逐渐减慢 | H+的浓度是影响反应速率的唯一因素 |
| B | 将形状大小相近的Mg和Al片分别放入相同浓度的盐酸中 | Mg与盐酸反应比Al剧烈 | Mg比Al的金属性强 |
| C | 氢气在氯气中点燃 | 有苍白色火焰,瓶口有白雾 | 其中 过程 过程吸收能量 |
| D | 将一小块钠投入冷水中 | 钠熔化成小球 |  |
| A. | A | B. | B | C. | C | D. | D |
分析 A.铝和酸的反应是放热反应,氢离子浓度、温度影响反应速率;
B.形状大小相近的Mg和Al片分别放入相同浓度的盐酸中,决定反应速率是物质本身性质;
C.氢气在氯气中燃烧时,形成化学键是放热反应;
D.钠和水的反应是放热反应.
解答 解:A.铝和酸的反应是放热反应,氢离子浓度、温度影响反应速率,铝表面含有氧化铝,氧化铝和稀盐酸反应较缓慢,铝和酸反应放出的热量导致温度升高,温度影响大于氢离子浓度影响,所以反应速率增大,当一段时间后,氢离子浓度对反应速率影响大于温度时,导致反应速率降低,故A错误;
B.形状大小相近的Mg和Al片分别放入相同浓度的盐酸中,决定反应速率是物质本身性质,Mg与盐酸反应比Al剧烈,所以Mg的金属性大于Al,故B正确;
C.氢气在氯气中燃烧时,形成化学键是放热反应,所以
D.钠和水的反应是放热反应,所以反应物能量大于生成物能量,故D错误;
故选B.
点评 本题考查化学实验方案评价,为高频考点,涉及反应热与能量关系、金属性强弱判断、化学反应速率影响因素等知识点,明确实验原理是解本题关键,注意:物质性质决定反应速率,外界只是影响因素,为易错点.


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:解答题
 化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置.
化学能和电能的相互转化,是能量转化的重要方式之一,如图两个实验装置是实现化学能和电能相互转化的装置.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 |  |  | 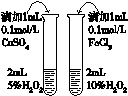 |
| 验证酸性: H2CO3>H2SiO3 | 用于分离CCl4萃取碘水后的有机层和水层 | 证明石蜡油分解生成的气体是乙烯 | 比较不同催化剂 对反应速率的影响 |
| A | B | C | D |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、SiO32-、Br- | B. | Na+、K+、CH3COO-、NO3- | ||
| C. | K+、Cl-、Fe3+、SO42- | D. | Mg2+、Al3+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 六氟合铝酸钠:Na3[AlF6] | B. | 氢氧化二氨合银:[Ag(NH3)2]OH | ||
| C. | 六氟合铁酸钾:K3[FeF6] | D. | 十二水硫酸铝钾:KAl(SO4)2•12H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com