
实验室用浓硫酸与铜的反应制取少量NaHSO3,实验装置如图所示:
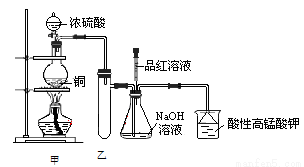
请回答:
(1)实验中取一定量Cu片和一定量浓H2SO4放在圆底烧瓶中共热,至反应结束后,发现烧瓶中还有少量Cu剩余,则H2SO4是否剩余________,原因是_____________ 。
①下列药品中,能够证明反应后烧瓶中有硫酸剩余的是________
A.Fe粉 B.BaCl2溶液 C.Ag D. 饱和NaHSO3溶液
②当向甲中反应后的溶液中通入氧气,发现铜片全部溶解,且仅生成硫酸铜溶液,则该反应的离子方程式为________________
(2)装置乙的作用是________________。
(3)请写出铜与浓硫酸反应的化学方程式___________________,浓硫酸在此反应中体现了_____________性质。
(4)下列说法正确的是________(填序号)。
a.甲装置使用的玻璃仪器有:酒精灯、玻璃管、长颈漏斗、圆底烧瓶
b.KMnO4溶液用于尾气处理
c.当把品红溶液滴入到锥形瓶中,若品红不褪色,说明无NaHSO3产生
d.当把品红溶液滴入到锥形瓶中,若品红褪色,说明NaOH已完全转化为NaHSO3
e.若把品红溶液换成酸性高锰酸钾溶液,并滴入到锥形瓶中,不显紫红色,说明NaOH已完全转化为NaHSO3
 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源:2016-2017学年天津市高一3月学生学业能力调研(文)化学试卷(解析版) 题型:选择题
关于P、S、Cl三种元素的说法不正确的是
A. 元素的非金属性 P>S>Cl
B. 最高价氧化物对应水化物的酸性 H3PO4<H2SO4<HClO4
C. 氢化物的稳定性 PH3<H2S<HCl
D. 原子半径 P>S>Cl
查看答案和解析>>
科目:高中化学 来源:2017届天津市河北区高三总复习质量检测 (一)化学试卷(解析版) 题型:选择题
下列离子方程式与所述事实相符且正确的是
A. 用H2O2酸性溶液,将海带灰中的I-转变为I2:H2O2+2I-=I2+2OH-
B. 漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3-
C. 工业电解熔融氯化钠制金属钠:2Na++2Cl- 2Na+Cl2↑
2Na+Cl2↑
D. Na2S2O3溶液中加入稀硫酸:2S2O32-+4H+=SO42-+3S↓+2H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二学业水平测试化学试卷(解析版) 题型:选择题
下列反应属于置换反应的是
A. Fe+CuSO4=FeSO4+Cu B. 2KClO3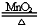 2KCl+3O2↑
2KCl+3O2↑
C. S+O2 SO2 D. NaOH+HCl=NaCl+H2O
SO2 D. NaOH+HCl=NaCl+H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高二学业水平测试化学试卷(解析版) 题型:选择题
下列诗句描述的过程包含化学变化的是
A. 千锤万凿出深山 B. 雪融山顶响流泉
C. 吹尽狂沙始到金 D. 蜡炬成灰泪始干
查看答案和解析>>
科目:高中化学 来源:2016-2017学年贵州省高一下学期第一次月考理科综合化学试卷(解析版) 题型:选择题
下列现象或事实可用同一原理解释的是( )
A. SO2和FeSO4溶液使酸性高锰酸钾的紫色褪去
B. 浓硫酸和浓盐酸长期暴露在空气中浓度降低
C. 不能用PH试纸测定浓硫酸和新制氯水的PH
D. 氢氧化钠固体易潮解和铝制容器可用盛装浓硫酸
查看答案和解析>>
科目:高中化学 来源:2017届河南省豫南九校高三下学期质量考评七理综化学试卷(解析版) 题型:填空题
钼酸钠晶体(Na2MoO4·2H2O)可用于制造生物碱、油墨、化肥、钼红颜料、催化剂等,也可用于制造阻燃剂和无公害型冷水系统的金属抑制剂。下图是利用钼精矿(主要成分是MoS2,含少量PbS等)为原料生产钼酸钠晶体的工艺流程图:

回答下列问题:
(1)Na2MoO4中Mo的化合价为____________。
(2)“焙烧”时,Mo元素转化为MoO3,反应的化学方程式为____________,氧化产物是________(写化学式)。
(3)“碱浸”生成CO2和另外一种物质,CO2的电子式为_______,另外一种生成物的化学式为______。
(4)若“除重金属离子”时加入的沉淀剂为Na2S,则废渣成分的化学式为________。
(5)测得“除重金属离子”中部分离子的浓度:c(MoO42-)=0.40mol/L,c(SO42-)=0.04mol/L。“结晶”前需先除去SO42-,方法是加入Ba(OH)2固体。假设加入Ba(OH)2固体后溶液体积不变,当BaMoO4开始沉淀时,SO42-的去除率为______%。(小数点后保留一位数字)[已知:Ksp(BaSO4)=1.1×10-10,Ksp(BaMoO4)=4.0×10-8]
(6)钼精矿在碱性条件下,加入NaClO溶液,也可以制备钼酸钠,同时有SO42-生成,该反应的离子方程式为___________________。
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江省哈尔滨市高三二模理科综合化学试卷(解析版) 题型:选择题
短周期元素X、Y、Z、W、R的原子序数依次增大,Y原子达到稳定结构获得的电子数目和它的内层电子数目相等,X与Z同主族,Z是所在周期主族元素中原子半径最大的元素,W的最外层电子数与电子层数相同,R与Z形成的化合物其水溶液呈碱性。下列说法正确的是
A. 离子半径由大到小的顺序为R、Z、Y、W
B. X、Y分别与Z形成的多种化合物在化学键类型都相同
C. 由X、Y、Z、R四种元素形成的两种化合物在水中不能发生反应
D. Z、W、R最高价氧化物对应的水合物两两之间均能发生反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二下学期第一次月考化学试卷(解析版) 题型:计算题
某有机物A与氢气的相对密度是30,取有机物A 6.0g完全燃烧后,生成0.2molCO2和0.2molH2O。此有机物既可与金属钠反应,又可与氢氧化钠和碳酸钠反应。
(1)计算该有机物的分子式。
(2)根据该有机物的性质,写出其结构简式。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com