
【题目】硝基苯可与金属Fe、盐酸反应生成苯胺和FeCl2,反应如下:
![]() +3Fe+6HCl
+3Fe+6HCl![]()
![]() +3FeCl2+2H2O
+3FeCl2+2H2O
(1)写出Fe2+基态核外电子排布式:_______。
(2)苯胺分子中C、N原子的杂化方式分别是________。1mol苯胺分子中含σ键的数目是___。
(3)苯胺与盐酸反应可生成氯化苯胺盐![]() ,氯化苯胺盐中含有的化学键有______。
,氯化苯胺盐中含有的化学键有______。
(4)苯胺在水中的溶解度大于硝基苯,其原因是________。
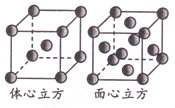
(5)金属铁单质的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。则两种晶胞中Fe原子的配位数之比为_______。
【答案】 [Ar]3d6 sp2 sp3 14NA 共价键、离子键、配位键(配位键可以不写) 苯胺分子与水分子间可以形成氢键 2:3
【解析】(1)铁是26号元素,其原子核外有26个电子,Fe原子的3d、4s电子为其价电子,则Fe2+核外有24个电子,排布式为[Ar]3d6,答案为:[Ar]3d6
(2)根据价层电子对互斥理论确定杂化类型,价层电子对个数=σ键个数+孤电子对,苯胺中碳原子杂化轨道数为3,所以采取sp2杂化,N元素全部形成单键,属于sp3杂化,单键都是σ键,1 mol苯胺分子中含σ键的数目是14NA故答案为:sp2 sp3,14NA
(3)氯化苯胺盐中含有共价键、离子键、配位键,故答案为:共价键、离子键、配位键。
(4)氢键比范德华力强,是一种介于化学键与分子间作用力之间的作用力,含F、O、N元素的物质中分子内或分子之间能形成氢键,苯胺在水中与水形成氢键,而硝基苯与水不能形成氢键,所以苯胺在水中的溶解度远大于硝基苯在水中的溶解度,故答案为:苯胺分子与水分子间可以形成氢键。
(5)体心立方晶胞中每个Fe原子周围有8个Fe原子,面心立方晶胞中,以顶点Fe原子为研究对象,与之最近的Fe原子处于面心,每个Fe原子周围有12个Fe原子,故体心立方晶胞和面心立方晶胞中Fe原子的配位数之比为8:12=2:3,故答案为:2:3.


科目:高中化学 来源: 题型:
【题目】常温下,下列说法不正确的是( )
A. 向滴有酚酞的Na2CO3溶液中加BaCl2固体,溶液红色变浅,则说明溶液中存在Na2CO3的水解平衡
B. 0.01mol/LCH3COOH溶液pH>2,说明CH3COOH为弱电解质
C. 含1molNH3H2O的溶液中加入HCl溶液,放出的热量小于57.3kJ,说明NH3H2O为弱电解质
D. 10mLpH=5的NH4Cl溶液稀释至1L,pH<7,则说明NH4Cl为弱电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于同分异构体的下列说法中正确的是
A. 结构不同,性质相同,化学式相同的物质互称同分异构体
B. 同分异构体现象是导致有机物数目众多的重要原因之一
C. 同分异构体现象只存在于有机化合物中
D. 同分异构体现象只存在于无机化合物中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下表数据(数据均为常温下所测数据),判断下列叙述正确的是( )

A. 在等浓度的NaClO、 NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)
B. 在等浓度的NaClO、NaHCO3混合溶液中:c(OH-)>c(HClO)>c(H2CO3)
C. 少量CO2通入NaClO溶液中反应的离子方程式为:CO2+H2O+2ClO—=CO32—+2HClO
D. 等温等浓度的NaClO溶液和NaHCO3溶液,前者导电能力强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若用AG表示溶液的酸度,其表达式为:AG=lgc(H+)/c(OH-)。室温下,实验室里用0.1mol/L的盐酸溶液滴定10mL0.1mol/LMOH溶液,滴定曲线如下图所示。下列说法正确的是

A. 该流定过程可选择酚酞作为指示剂
B. 溶液中由水电离的c(H+):C点>D点
C. C点时加入盐酸溶液的体积等于10mL
D. 若B点加入的盐酸溶液体积为5mL,所得榕液中:c(M+)+c(H+)=c(MOH)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是( S-32 O-16 ) ( )
A.标准状况下,22.4L氦气含有2NA个氦原子
B.在常温常压下,11.2L Cl2含有的分子数为0.5NA
C.常温常压下,64g SO2中含有的氧原子数为2NA
D.标准状况下,11.2LH2O含有的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,人类生产、生活所产生的污染使灰霾天气逐渐增多。灰霾粒子的平均直径在1000nm~2000nm。下列有关说法正确的是
A. 灰霾可能来自汽车尾气 B. 灰霾属于胶体
C. 灰霾形成的是非常稳定的体系 D. 戴口罩不能阻止呼入灰霾粒子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com