

| n(Fe3+) |
| n(Fe2+) |
| n(Fe3+) |
| n(Fe2+) |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、常温常压下,22.4LCO2中含有NA个CO2分子 |
| B、1.7 gH2O2中含有电子数为0.9NA |
| C、标准状况下,2.24LH2O含有的分子数等于0.1NA |
| D、分子总数为NA的CO和C2H4混合气体体积约为22.4L则质量为28g |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将106gNa2CO3溶于100mL水中 |
| B、含3molO的硝酸溶于水得100mL溶液 |
| C、从2L物质的量浓度为1mol/L的NaCl溶液中取出100mL溶液 |
| D、22.4LHCl气体溶于水得1L溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④ | B、②③④ |
| C、①③④ | D、④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
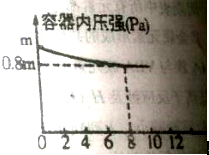
查看答案和解析>>
科目:高中化学 来源: 题型:

| NaOH/H2O |
| H+ |
| Fe/HCl |

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、工业上用铁矿石炼铁 |
| B、用稀盐酸除去钢铁表面的铁锈 |
| C、工业上煅烧石灰石制生石灰 |
| D、用胃舒平(氢氧化铝)治疗胃酸过多 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com