
【题目】下列热化学方程式中,正确的是( )
A.甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H = -38.6kJ·mol-1
2NH3(g) △H = -38.6kJ·mol-1
C.HCl和NaOH 反应的中和热△H= -57.3kJ·mol-1,则H2SO4和Ba(OH)2反应的热化学方程式为:H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) △H=-114.6kJ·mol -1
D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,H2燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(1) △H =-571.6kJ·mol-1
【答案】D
【解析】
A.甲烷的燃烧热为890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-890.3kJmol-1,A错误;
B.合成氨为可逆反应,0.5molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,则1molN2完全反应时放热大于38.6kJ,热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H <-38.6kJ·mol-1,B错误;
2NH3(g) △H <-38.6kJ·mol-1,B错误;
C.HCl和NaOH 反应的中和热△H= -57.3kJ·mol-1,H2SO4和Ba(OH)2反应,除产生2molH2O外,还形成BaSO4沉淀,会放出热量,所以反应放出热量大于114.6kJ,故反应的热化学方程式为:H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) △H<-114.6kJ·mol -1,C错误;
D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,2molH2燃烧放出热量为2×285.8kJ =571.6kJ,故H2燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(1) △H =-571.6kJ·mol-1,D正确;
故合理选项是D。


 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案科目:高中化学 来源: 题型:
【题目】中枢神经兴奋剂芬坎法明的合成路线如下:
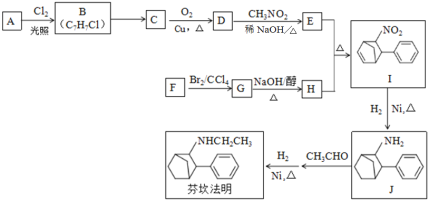
已知:i、![]() (R、
(R、![]() 表示烃基或氢)
表示烃基或氢)
ii、![]()
请回答:
(1)A属于芳香烃,名称是______。
(2)J中所含官能团是______。
(3)C→D的化学方程式是______。
(4)E具有反式结构,其结构简式是______。
(5)H是五元环状化合物,G→H的化学方程式是________。
(6)1mol![]() 转化为
转化为![]() ,同时生成H2O,理论上需要H2的物质的量是_____mol。
,同时生成H2O,理论上需要H2的物质的量是_____mol。
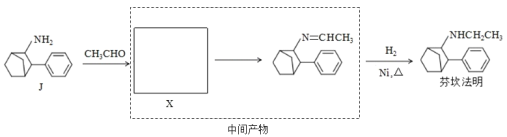
(7)J→芬坎法明的转化过程中,中间产物X可能的结构简式是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与化学有关的文献,理解正确的是
A. 《石灰吟》中“…烈火焚烧若等闲…要留清白在人间”,其中“清白”指氢氧化钙
B. 《咏煤炭》中“凿开混沌得乌金…不辞辛苦出山林”,其中“乌金”的主要成分是木炭
C. 《本草纲目》中“冬月灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣”,其中的“碱”是一种盐溶液
D. 《天工开物》中有如下描述:“世间丝、麻、裘、褐皆具素质…”文中的“丝”“麻”、“裘”主要成分均属于多糖
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟碳铈矿(主要成分为CeFCO3)是提取稀土化合物、冶炼铈的重要矿物原料,以氟碳铈矿为原料提取铈的工艺流程如图所示。回答下列问题:

(1)CeFCO3中Ce的化合价为______。
(2)氧化焙烧后的产物之一为CeO2,则酸浸时发生反应的离子方程式为________。
(3)HT是一种难溶于水的有机溶剂,则操作Ⅰ的名称为_____。
(4)为了提高酸浸率,可以适当提高反应温度,但温度偏高浸出率反而会减小,其原因是___________。
(5)有机物HT能将Ce3+从水溶液中提取出来,该过程可表示为Ce3+ (水层)+3HT(有机层)![]() CeT3 (有机层)+3H+ (水层)。向CeT3(有机层)中加入稀硫酸能获得较纯的含Ce3+水溶液,从平衡角度解释其原因:_________。
CeT3 (有机层)+3H+ (水层)。向CeT3(有机层)中加入稀硫酸能获得较纯的含Ce3+水溶液,从平衡角度解释其原因:_________。
(6)已知,298K时,Ksp[Ce(OH)3]=5×l0-20,若溶液中c(Ce3+)=0.05mol·L-1,加碱调节pH到_____时Ce3+开始沉淀(忽略加碱过程中溶液体积变化)。
(7) 写出向Ce(OH)3悬浊液中通入氧气得到产品Ce(OH)4的化学方程式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2CO2+6H2 ![]() CH2=CH2+4H2O可用于合成烯烃。下列有关说法错误的是
CH2=CH2+4H2O可用于合成烯烃。下列有关说法错误的是
A. 增大压强可加快该反应速率
B. 降低温度能减慢该反应速率
C. 增大H2的浓度能加快该反应速率
D. 若反应中加入足量的H2,可使CO2 100% 转化为CH2=CH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增大,W、Z位于同主族,四种元素组成的一种化合物的结构式为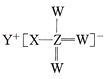 。下列说法不正确的是
。下列说法不正确的是
A. W的最简单氢化物的稳定性比X的弱
B. X.Y形成的化合物水溶液显碱性
C. W与Y形成的化合物中一定含有离子键
D. 原子半径:Y>Z>X>W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中是可逆反应X2+3Y2![]() 2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是
2Z2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是

A. t1时,只有正向进行的反应 B. t1~t2,X2的物质的量越来越多
C. t2~t3,反应不再发生 D. t2~t3,各物质的浓度不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为减少交通事故,新交规明令禁止酒后驾车并对酒后驾车行为予以重罚。为检验驾驶员是否酒后驾车,可采用的检验方法有多种。回答以下问题:
(1)早期曾经采用五氧化二碘和某种高分子化合物X的混合溶液来检测酒精的存在。其原理是:I2O5与CH3CH2OH先发生反应(I2O5+5CH3CH2OH=I2+5Y+5H2O),生成的I2与高分子化合物X作用而变蓝。交警依据此原理来检测驾驶员是否饮酒。则:
X的化学名称是__________;
Y的分子式是____________;
(2)已知:I2O5是白色固体,可用于检验并定量测定空气中CO;两者在常温条件下发生的反应为5CO+I2O5=5CO2+I2(空气中其余气体不与I2O5反应);某同学设计如右实验装置完成上述目的。
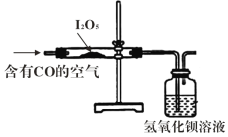
①指出能证明空气中有CO存在的现象。答:__________________________。
②将上述反应生成的碘单质用硫代硫酸钠滴定(反应为I2+2Na2S2O3=Na2S4O6+2NaI),即可根据消耗硫代硫酸钠的量来计算空气中CO的含量。若某次实验时测得参与反应的空气体积为a mL(标准状况下),滴定过程中,共消耗vmL c mol·L-1Na2S2O3溶液。则该空气样品中CO的体积分数是_____________。
③有同学提出只要依据参与反应的空气体积和洗气瓶中白色沉淀的质量也可求得空气中CO的体积分数。此方案是否可行?答:_________________________。
(3)燃料电池酒精检测仪(该电池以硫酸溶液为电解质溶液)也是检测酒精含量的一种方法。总反应是:CH3CH2OH+O2=CH3COOH+H2O。该电池正极电极反应式是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:X(g)+3Y(g)![]() 2Z(g),有关下列图像的说法错误的是( )
2Z(g),有关下列图像的说法错误的是( )

A. 依据图甲可判断正反应为放热反应
B. 在图乙中,虚线可表示使用了催化剂
C. 若正反应的△H<0,图丙可表示升高温度使平衡向逆反应方向移动
D. 由图丁中气体平均相对分子质量随温度的变化情况,可推知正反应的△H >0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com