
| A、铁溶于稀硝酸,溶液变为浅绿色:Fe+4H++NO3-═Fe3++NO↑十2H2O |
| B、用KIO3氧化酸性溶液中的KI:5I-+IO3-+3H2O═3I2+6OH- |
C、向水杨酸(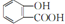 )中滴加NaHCO3溶液,放出无色气体: )中滴加NaHCO3溶液,放出无色气体: |
| D、0.01mol?L-1 NH4Al(SO4)2溶液与0.02mol?L-1 Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3?H2O |
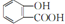 )中滴加NaHCO3溶液,只有羧基的酸性比碳酸的酸性强,而酚羟基的酸较碳酸要弱得多,所以酚羟基与NaHCO3溶液不反应;
)中滴加NaHCO3溶液,只有羧基的酸性比碳酸的酸性强,而酚羟基的酸较碳酸要弱得多,所以酚羟基与NaHCO3溶液不反应;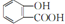 )中滴加NaHCO3溶液,放出无色气体,正确的离子反应为
)中滴加NaHCO3溶液,放出无色气体,正确的离子反应为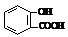 +HCO3-→
+HCO3-→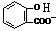 +CO2↑+H2O,故C错误;
+CO2↑+H2O,故C错误;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 体积/mL | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 离子方程式 | 评价 |
| A | 将1mol Cl2通入到含1mol FeI2的溶液中: 2Fe2++2I-+2Cl2=2Fe3++4Cl-+I2 | 正确;Cl2过量,可将 Fe2+、I-均氧化 |
| B | Mg(HCO3)2溶液与足量的NaOH溶液反应: Mg2++HCO3-+OH-=MgCO3↓+H2O | 正确;酸式盐与碱反应 生成正盐和水 |
| C | 过量SO2通入到NaClO溶液中: SO2+H2O+ClO-=HClO+HSO3- | 正确; 说明酸性: H2SO3强于HClO |
| D | 1mol/L的NaAl(OH)4溶液和2.5mol/L的HCl溶 液等体积互相均匀混合:2[Al(OH)4]-+5H+=Al3++Al(OH)3↓+5H2O | 正确:[Al(OH)4]-与Al(OH)3消耗的H+的物 质的量之比为2:3 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 可逆反应:Cr2O72-+H2O?2CrO42-+2H+达平衡状态溶液呈橙黄色,滴加少量的浓硝酸,溶液变橙色,氢离子浓度随时间变化曲线如图 |
B、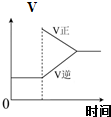 可逆反应Co(H2O)62+(粉红色)+4Cl-?CoCl42-(蓝色)+6H2O达平衡状态溶液呈紫色,升高温度,溶液变蓝色,反应速率随时间变化曲线如图 |
C、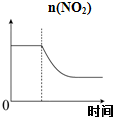 可逆反应:2NO2?N2O4达平衡状态呈红棕色,加压(缩小体积)红棕色变深,NO2物质的量随时间变化曲线如图 |
D、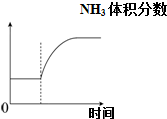 可逆反应:N2(g)+3H2(g)?2NH3(g)△H<0达平衡状态,升高温度,NH3体积分数随时间变化曲线如图 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、使用催化剂可以提高SO2的转化率 |
| B、增大O2的浓度可以提高反应速率和SO2的转化率 |
| C、反应450℃时的平衡常数小于500℃时的平衡常数 |
| D、2mol SO2(g)和1mol O2(g)所含的总能量小于2mol SO3(g)所含的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某物质的溶液pH<7,则该物质一定是酸或强酸弱碱盐 | ||
| B、pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的102倍 | ||
| C、常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为1×10-24,该溶液中一定可以大量存在K+、Na+、AlO2-、SO42- | ||
D、常温时,0.1mol/L HA溶液的pH>1,0.1mol/L BOH溶液中
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c (Na+)=c (HCO3-)+c (CO32-)+c (H2CO3) |
| B、c (Na+)+c (H+)=c (HCO3-)+c (CO32-)+c (OH-) |
| C、HCO3- 的电离程度大于HCO3-的水解程度 |
| D、存在的电离平衡有:HCO3-?H++CO32-,H2O?H++OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 能源是人类生存和发展的重要支柱.研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义.已知下列热化学方程式
能源是人类生存和发展的重要支柱.研究化学反应过程中的能量变化在能源紧缺的今天具有重要的理论意义.已知下列热化学方程式| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com